题目内容
水是一种重要的物质,在日常生活生产和实验室中有着不可替代的作用.回答下列问题:
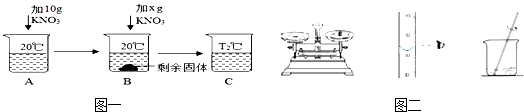
(1)如图一所示,向50g水中加KNO3固体(已知20℃时KNO3的溶解度为31.6g/100g水),当B中KNO3加到 g时,B恰好饱和;图示中B到C的操作可以是 .
(2)若按照图二所示的操作配制10%的食盐溶液,则配制的食盐溶液的浓度会 10%.(填“大于”、“小于”或“等于”)
(3)高铁酸钾(K2FeO4)是一种新型高效的水处理剂,高铁酸钾受热时会发生反应如下:4K2FeO4 2X+4K2O+3O2↑,生成物X的化学式是 ,K2FeO4→O2中氧元素由 态变成 态.
2X+4K2O+3O2↑,生成物X的化学式是 ,K2FeO4→O2中氧元素由 态变成 态.
(4)海水通常含泥沙和可溶性杂质,净化海水需采取的措施是 (填编号).
A.沉降 B.过滤 C.吸附 D.蒸馏.
【考点】饱和溶液和不饱和溶液;一定溶质质量分数的溶液的配制;过滤的原理、方法及其应用;单质和化合物的判别;质量守恒定律及其应用.
【专题】化学用语和质量守恒定律;溶液、浊液与溶解度;物质的分类.
【分析】(1)根据已有的知识进行分析,在一定温度下,在一定量的溶剂里不能再溶解某种固体的溶液,叫做这种溶质在这种溶剂里的饱和溶液,还能溶解的叫不饱和溶液,据此解答;
(2)根据配置一定溶质质量分数的溶液,用量筒量水时,读取量筒内液体体积时,视线应与液体凹液面的最低处保持水平,俯视读数会导致所量取的液体实际体积小于所量值,仰视读数会导致所量取的液体实际体积大于所量值进行分析;
(3)根据质 量守恒定律,反应前后原子的种类及数目不变分析R的化学式;
量守恒定律,反应前后原子的种类及数目不变分析R的化学式;
【解答】解:(1)在20℃时,硝酸钾的溶解度是31.6g,则20℃时100g水中最多溶解硝酸钾的质量是31.6g,故x=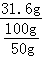 ﹣10g=5.8g;据图可以看出,B中有固体而C中没有,故B升可通过升温变为C溶液也可能是过滤出去了不溶性固体;
﹣10g=5.8g;据图可以看出,B中有固体而C中没有,故B升可通过升温变为C溶液也可能是过滤出去了不溶性固体;
(2)通过分析可知,配置10%的食盐溶液,用量筒量水时,俯视刻度,会导致所量取的液体实际体积小于所量值,即所量取的水的实际体积偏小,质量偏少,溶质质量不变,所以所得溶液的质量分数大于10%.
(3)根据反应的化学方程式4K2FeO4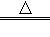 2R+4K2O+3O2↑,反应物中钾、铁、氧原子个数分别为8、4、16,反应后的生成物中钾、铁、氧原子个数分别为8、0、10,根据反应前后原子种类、数目不变,则2R中含有4个铁原子和6个氧原子,则每个R分子由2个铁原子和3个氧原子构成,则物质R的化学式为Fe2O3.K2FeO4→O2中氧元素由化合态变为了游离态;
2R+4K2O+3O2↑,反应物中钾、铁、氧原子个数分别为8、4、16,反应后的生成物中钾、铁、氧原子个数分别为8、0、10,根据反应前后原子种类、数目不变,则2R中含有4个铁原子和6个氧原子,则每个R分子由2个铁原子和3个氧原子构成,则物质R的化学式为Fe2O3.K2FeO4→O2中氧元素由化合态变为了游离态;
(4)海水通常含 泥沙和可溶性杂质,净化海水需采取的措施是现沉降除去较大的不溶性颗粒杂质,再过滤出去所有的不溶性杂质,再用活性炭吸附出去颜色和异味杂质,最后蒸馏得到纯净水;
泥沙和可溶性杂质,净化海水需采取的措施是现沉降除去较大的不溶性颗粒杂质,再过滤出去所有的不溶性杂质,再用活性炭吸附出去颜色和异味杂质,最后蒸馏得到纯净水;
答案:(1)5.8; 升温或过滤; (2)大于; (3)Fe2O3; 化合; 游离;
(4)ABCD.
【点评】本题考查了饱和溶液的有关知识,以及根据溶解度的计算,完成此题,可以依据已有的知识进行.本题考查了饱和溶液的有关知识,以及根据溶解度的计算,完成此题,可以依据已有的知识进行.

除去下列物质中的少量杂质所用的药品或方法正确的是( )
| 选项 | 物质 | 杂质 | 除杂药品或方法 |
| A | CO2 | CO | 点燃 |
| B | MnO2 | KCl | 加足量水、过滤 |
| C | CaO | CaCO3 | 加足量水、过滤 |
| D | Fe | C | 氧气流中加热 |
A.A B.B C.C D.D
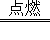 2MgO+C中作还原剂的物质是( )
2MgO+C中作还原剂的物质是( ) 是一门自然科学,研究和发展化学科学的基础是( )
是一门自然科学,研究和发展化学科学的基础是( ) X+N2↑+3CO2↑,则X的化学式是( )
X+N2↑+3CO2↑,则X的化学式是( )