题目内容
17.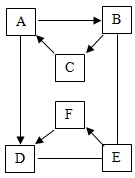 有A-F六种物质,已知A、B、C三种固体含有同种金属元素,A是大理石、石灰石的主要成分,B是一种氧化物能与E反应放出大量的热,D、E、F含有同种非金属元素,E通常状况下为液体,D、F通常状况下为气体,且F为单质.它们的转化关系如图(部分产物已略去).温馨提示:图中“→”表示箭尾的物质可转化为箭头的物质;“-”表示两端的物质能发生化学反应.
有A-F六种物质,已知A、B、C三种固体含有同种金属元素,A是大理石、石灰石的主要成分,B是一种氧化物能与E反应放出大量的热,D、E、F含有同种非金属元素,E通常状况下为液体,D、F通常状况下为气体,且F为单质.它们的转化关系如图(部分产物已略去).温馨提示:图中“→”表示箭尾的物质可转化为箭头的物质;“-”表示两端的物质能发生化学反应.(1)写出A、E物质的名称:A碳酸钙;E水
(2)写出C→A的化学方程式:Ca(OH)2+CO2═CaCO3↓+H2O
(3)写出E→F的化学方程式:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
分析 根据题干提供的信息进行分析解答,A、B、C三种固体含有同种金属元素,A是大理石、石灰石的主要成分,故A是碳酸钙;B是一种氧化物能与E反应放出大量的热,E通常状况下为液体,故B是氧化钙,E是水;C是氢氧化钙;碳酸钙能反应生成D,D为气体,故D是二氧化碳,F为单质,能由水生成,且能生成二氧化碳,故F是氧气,据此解答.
解答 解:A、B、C三种固体含有同种金属元素,A是大理石、石灰石的主要成分,故A是碳酸钙;B是一种氧化物能与E反应放出大量的热,E通常状况下为液体,故B是氧化钙,E是水;C是氢氧化钙;碳酸钙能反应生成D,D为气体,故D是二氧化碳,F为单质,能由水生成,且能生成二氧化碳,故F是氧气,带入框图,推断合理;
(1)A是碳酸钙,E是水,故填:碳酸钙;水;
(2)C是氢氧化钙,A是碳酸钙,氢氧化钙能与二氧化碳反应生成碳酸钙沉淀和水,故填:Ca(OH)2+CO2═CaCO3↓+H2O;
(3)水通电分解生成氢气和氧气,故填:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
点评 本题属于框图式推断题,解题的关键是照准推断的突破口,根据物质的性质和转化关系逐渐得出结论,然后带入验证即可.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
5.节日期间的商场里人头攒动,常常会让人感觉闷热缺氧.此时,测定出氧气的体积分数可能是( )
| A. | 1% | B. | 75% | C. | 25% | D. | 19% |
12.比较、推理是化学学习常用的方法,以下是根据一些反应事实推导出的影响化学反应的因素,其中推理合理的是:( )
| 序号 | 化学反应事实 | 影响化学反应的因素 |
| ① | 硫在氧气中燃烧,比在空气中燃烧更剧烈 | 反应物浓度 |
| ② | 碳在常温下不与氧气发生,而在点燃时能与氧气 | 反应物温度 |
| ③ | 过氧化氢溶液在常温下较难分解,而在加入二氧化锰后迅速分解 | 催化剂 |
| ④ | 铁丝在空气中很难燃烧,而在氧气中能剧烈燃烧 | 反应物种类 |
| ⑤ | 碳充分燃烧时生成二氧化碳,不充分燃烧时生成一氧化碳 | 反应物的量 |
| A. | 2个 | B. | 3个 | C. | 4个 | D. | 5个 |
