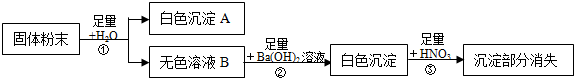
题目内容
8.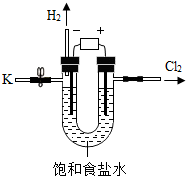 某学习小组对课本中“食盐常用于制氯气、烧碱”的内容产生兴趣.在老师的指导下,用自制的实验装置(主体部分如图所示)进行电解饱和食盐水制取氢氧化钠的实验.一段时间后,关闭电源,从K处导出一定量的溶液作为待测液进行如下探究.
某学习小组对课本中“食盐常用于制氯气、烧碱”的内容产生兴趣.在老师的指导下,用自制的实验装置(主体部分如图所示)进行电解饱和食盐水制取氢氧化钠的实验.一段时间后,关闭电源,从K处导出一定量的溶液作为待测液进行如下探究.老师提示:
Ⅰ.电解饱和食盐水的化学方程式:2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$ 2NaOH+H2↑+Cl2↑
Ⅱ.忽略其他可能发生的反应对本实验的影响.
探究活动一:检验待测液中含有氢氧化钠
(1)同学们选用某种酸碱指示剂对待测液进行检验,确定待测液中含有氢氧化钠.
探究活动二:测定待测液中氢氧化钠的质量分数
【实验1】用酸碱中和法测定
甲组同学称取一定质量的待测液于烧杯中,加水稀释,用带有刻度的滴管逐滴加入
一定溶质质量分数的稀盐酸,边加边振荡,用pH计测定溶液的pH,所得数据如下:
| 加入稀盐酸的体积/mL | 0 | 2.0 | 4.0 | 6.0 | 8.0 | 9.8 |
| 烧杯中溶液的pH | 13.0 | 12.9 | 12.8 | 12.6 | 12.3 | 7.0 |
【实验2】用沉淀法测定
资料摘要:氢氧化钠与氯化镁在溶液中发生反应:2NaOH+MgCl2=Mg(OH)2↓+2NaCl.
乙组同学按下图所示的实验步骤进行实验:
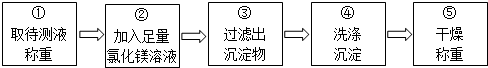
(3)步骤②加入的氯化镁溶液必需足量,其目的是使氢氧化钠完全反应.
(4)步骤③过滤出的沉淀物是氢氧化镁.
(5)利用沉淀物的质量计算氢氧化钠的质量分数,若缺少步骤④的操作,所测定氢氧化钠的质量分数将偏大(选填“偏大”、“偏小”或“没影响”).
分析 (2)氢氧化钠和稀盐酸反应,如果溶液的pH=7时,说明氢氧化钠和稀盐酸恰好完全反应;
(3)为了使氢氧化钠完全反应,加入的氯化镁溶液必须足量或过量;
(4)氢氧化镁不溶于水;
(5)如果不洗涤沉淀物,会导致测定的质量偏大.
解答 解:(2)当稀盐酸的体积为9.8mL时,溶液的pH=7,说明氢氧化钠和稀盐酸恰好完全反应,因此计算所称取待测液中氢氧化钠的质量,应从选用稀盐酸的体积为9.8mL.
故填:9.8.
(3)步骤②加入的氯化镁溶液必需足量或过量,其目的是使氢氧化钠完全反应;
故填:使氢氧化钠完全反应;
(4)步骤③过滤出的沉淀物是氢氧化镁.
故填:氢氧化镁.
(5)利用沉淀物的质量计算氢氧化钠的质量分数时,若缺少步骤④的操作,会导致测定的氢氧化镁质量偏大,从而导致计算的氢氧化钠的质量偏大,会使所测定氢氧化钠的质量分数偏大.
故填:偏大.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
16.氢氧化钠的俗称不止一个,下列俗名不表示氢氧化钠的是( )
| A. | 苛性钠 | B. | 石灰石 | C. | 烧碱 | D. | 火碱 |
13.下列化学实验基本操作正确的是( )
| A. |  点燃酒精灯 | B. | 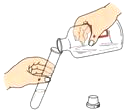 液体取用 | C. | 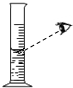 量取液体 | D. | 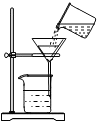 过滤 |
20.生活中处处有化学,在实际生活中下列物质的用途只与其物理性质有关的是( )
| A. | 二氧化碳做灭火剂 | |
| B. | 酒精用于给发烧病人擦拭以降低温度 | |
| C. | 氦气用作食品防腐剂 | |
| D. | 二氧化碳做温室的气体肥料 |
17.向一定量的稀盐酸中加入过量铁粉,下列示意图正确的是( )
| A. | 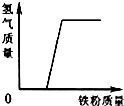 | B. | 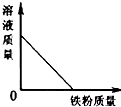 | C. | 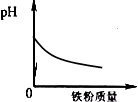 | D. | 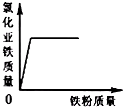 |