题目内容
9.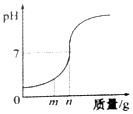 用氢氧化钠中和一定量的硫酸时,溶液的pH与加入的氢氧化钠质量的关系如图所示.氢氧化钠与硫酸反应的化学方程式为2NaOH+H2SO4=Na2SO4+2H2O;当加入氢氧化钠mg时,溶液中的溶质为Na2SO4和H2SO4,若改用ng熟石灰与相同量硫酸反应,所得溶液的pH>7(填“>”“<”或“=”).
用氢氧化钠中和一定量的硫酸时,溶液的pH与加入的氢氧化钠质量的关系如图所示.氢氧化钠与硫酸反应的化学方程式为2NaOH+H2SO4=Na2SO4+2H2O;当加入氢氧化钠mg时,溶液中的溶质为Na2SO4和H2SO4,若改用ng熟石灰与相同量硫酸反应,所得溶液的pH>7(填“>”“<”或“=”).
分析 氢氧化钠与硫酸反应生成硫酸钠与水,写出反应的化学方程式即可.根据图象中pH值的变化是从小于7逐渐的增大到大于7,当加入溶液的质量为mg时,溶液的pH小于7,据此进行分析解答.根据质量守恒定律可以书写化学方程式,根据化学方程式和图中情况可以进行相关方面的计算.
解答 解:氢氧化钠和硫酸反应能生成硫酸钠和水,化学方程式为:2NaOH+H2SO4=Na2SO4+2H2O;故填:2NaOH+H2SO4=Na2SO4+2H2O;
当加入氢氧化钠mg时,溶液的pH<7,显酸性,即硫酸有剩余,溶液中的溶质是硫酸和反应生成的硫酸钠.故填:Na2SO4和H2SO4;
当加到ng氢氧化钠时,氢氧化钠与硫酸签好完全中和,若改用ng氢氧化钙,由化学方程式:
Ca(OH)2+H2SO4=CaSO4+2H2O;
74 98
2NaOH+H2SO4=Na2SO4+2H2O
80 98
可知,消耗等质量的硫酸需要的氢氧化钠的质量较大,所以若改用ng氢氧化钙与相同质量硫酸反应,氢氧化钙过量,溶液显碱性,则溶液的pH>7;故填:>.
点评 本题难度不大,主要考查了中和反应及其应用,掌握溶液的酸碱性和溶液pH大小之间的关系、从数形结合的角度理解中和反应是正确解答本题的关键.

练习册系列答案
 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目
3.保护环境,人人有责.下列建议不可行的是( )
| A. | 严禁随意焚烧秸秆,减少PM2.5排放 | |
| B. | 开发和使用太阳能、风能、减少化石燃料使用 | |
| C. | 分类回收垃圾,以促进资源再生的利用 | |
| D. | 禁止使用化肥和农药,以防止水体污染 |
17.物质的微观结构知识可以解释其宏观现象或事实,下列现象及事实与相应的解释不一致的是( )
| 现 象 及 事 实 | 解 释 | |
| A | 医用酒精敞口放置一段时间后,浓度变稀 | 分子是运动的 |
| B | 酒精燃烧后变成生成二氧化碳气体和水蒸气 | 分子间隔变大了 |
| C | 测出氢氧化钠溶液pH>7,其溶液显碱性 | 溶液中存在大量OH- |
| D | 不同的花儿有不同的香味 | 不同的分子性质不同 |
| A. | A | B. | B | C. | C | D. | D |
1.淮南豆腐制作工艺驰名中外,下列手工制作豆腐的步骤中发生化学变化的是( )
| A. |  磨浆 | B. |  滤渣 | C. |  煮浆 | D. |  成型 |
18.下列化学方程式书写完全正确的是( )
| A. | 4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 | B. | 2KClO3$\frac{\underline{\;MnO_2\;}}{\;}$2KCl+O2↑ | ||
| C. | C+CO2$\frac{\underline{\;高温\;}}{\;}$2CO | D. | Fe+ZnCl2═Zn+FeCl2 |
 同学们在实验室看到有一瓶没有盖瓶塞的硫酸,欲测量这瓶硫酸的质量分数,现取50g该硫酸溶液倒入烧杯中,再向该烧杯中滴加17.1%的Ba(OH)2溶液,测量的pH与滴加Ba(OH)2溶液之间的关系如图所示:
同学们在实验室看到有一瓶没有盖瓶塞的硫酸,欲测量这瓶硫酸的质量分数,现取50g该硫酸溶液倒入烧杯中,再向该烧杯中滴加17.1%的Ba(OH)2溶液,测量的pH与滴加Ba(OH)2溶液之间的关系如图所示:
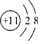 .
. C919中,“C”是中国英文名称China的首字母.在化学中,“C”也代表碳元素,碳纤维材料在航空、航天、航海中也有着广泛应用,如图是元素周期表中的碳元素.
C919中,“C”是中国英文名称China的首字母.在化学中,“C”也代表碳元素,碳纤维材料在航空、航天、航海中也有着广泛应用,如图是元素周期表中的碳元素.