题目内容
实验室可用高锰酸钾与浓盐酸反应制取氯气,反应的化学方程式为:2KMnO4+16HCl(浓)═2KCl+2MnCl2+8X+5Cl2↑,其中X的化学式为( )
|
| A. | H2O | B. | H2O2 | C. | HClO | D. | O2 |
| 质量守恒定律及其应用.菁优网版权所有 | |
| 专题: | 化学用语和质量守恒定律. |
| 分析: | 化学反应前后,元素的种类不变,原子的种类、总个数不变. |
| 解答: | 解:由2KMnO4+16HCl(浓)═2KCl+2MnCl2+8X+5Cl2↑可知, 反应前钾原子是2个,反应后是2个; 反应前锰原子是2个,反应后是2个; 反应前氧原子是8个,反应后应该是8个,包含在8X中; 反应前氢原子是16个,反应后应该是16个,包含在8X中; 反应前氯原子是16个,反应后是16个; 由分析可知,每个X中含有2个氢原子和1个氧原子,是水,水的化学式是H2O. 故选:A. |
| 点评: | 化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、进行相关方面计算的基础. |

氧循环和碳循环密不可分,其中属于二氧化碳转化为氧气的变化是( )
|
| A. | 海水吸收二氧化碳 | B. | 动植物的呼吸作用 |
|
| C. | 绿色植物的光合作用 | D. | 化石燃料的燃烧 |
物质分类是一种重要的化学思想.下列物质中属于酸的是( )
|
| A. | H2CO3 | B. | NaHCO3 | C. | P2O5 | D. | KOH |
下列几种粒子的结构示意图中表示阴离子的是( )
|
| A. |
| B. |
| C. |
| D. |
|
一种名为“污渍爆炸盐”的洗涤产品能高效去除衣物上的顽固污渍,某校化学研究性学习小组的同学在老师的指导下对该产品开展了以下探究活动.
【查阅资料】
“污渍爆炸盐”的主要成分是过碳酸钠(相对分子质量为122),它是一种白色固体粉末,易溶于水且能与水反应生成一种碳酸盐和一种强氧化性的物质,是当前使用最为广泛的洗涤助剂之一.
【实验探究一】过碳酸钠的化学组成
为探究过碳酸钠的化学组成,同学们设计了以下实验,请按要求完成表格内容:
| 序号 | 实验步骤 | 实验现象[来源:学*科*网] | 实验分步结论(或解释) |
| ① | 向盛有过碳酸钠固体的试管中加入适量水 | 固体溶解 |
.[来源:学&科&网Z&X&X&K] |
| ② | 向序号①的所得溶液中加入适量的二氧化锰粉末 | 有大量气泡产生 |
|
| ③ | 将带火星的木条置于试管口 | 木条复燃 | 序号②试管中产生的气体是 ;过碳酸钠溶于水能生成 (填化学式). |
| ④ | 取序号 | 产生白色沉淀 |
反应的化学方程式 . |
| 实验 小结 | 过碳酸钠的化学式是 ; 过碳酸钠与水反应的化学方程式是 . |
【实验探究二】:过碳酸钠含量测定
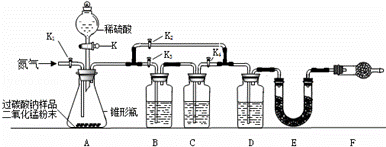
老师给同学们一份含碳酸钠杂质的过碳酸钠样品(不含其它杂质 ),要求设计方案测定该样品中过碳酸钠的含量,同学们经讨论设计了如图所示的实验装置.图中装置B盛装氢氧化钠溶液、C盛装澄清石灰水、D盛装浓硫酸,E、F均装入干燥的碱石灰(主要成分:氧化钙和氢氧化钠的固体混合物;可吸收二氧化碳和水蒸气).
),要求设计方案测定该样品中过碳酸钠的含量,同学们经讨论设计了如图所示的实验装置.图中装置B盛装氢氧化钠溶液、C盛装澄清石灰水、D盛装浓硫酸,E、F均装入干燥的碱石灰(主要成分:氧化钙和氢氧化钠的固体混合物;可吸收二氧化碳和水蒸气).
(1)首先关闭活塞K、K2,打开活塞K1、K3、K4,通入一段时间的氮气排出锥形瓶中的空气,此时装置B的作用是 ;
(2)依次关闭活塞K1、K3、K4,打开活塞K2、K,此时锥形瓶中反应生成的气体是 ,E中装入碱石灰的作用是 ,反应完全后关闭活塞K,再次打开活塞K1通 入氮气的作用是 ;
入氮气的作用是 ;
(3)同学们根据E装置在测定前后的质量差计算出了样品中过碳酸钠的含量.装置F的作用是 ,如不连接装置F,测定的过碳酸钠含量会 (填“偏高”或“偏低”).
下列对一些现象或事实解释不正确的是( )
| 序号 | 现象或事实 | 解释 |
| A | 洒在地面上的酒会使房间充满酒味 | 分子在不断运动 |
| B | 酸都具有相似化学性质 | 溶于水时都能解离出氢离子 |
| C | 物质的热胀冷缩 | 分子或原子的大小随温度改变而改变 |
| D | 铵态氮肥与碱性物质混用,降低肥效 | 铵盐与碱反应放出氨气 |
A. A B. B C. C D. D
 ;②氯化钠是由 构成的;③镁是
;②氯化钠是由 构成的;③镁是 的;④化学变化中的最小粒子是 。
的;④化学变化中的最小粒子是 。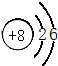




 氧化钠溶液
氧化钠溶液