题目内容
 100克某浓度的硫酸恰好与13克的锌完全起反应,请计算:
100克某浓度的硫酸恰好与13克的锌完全起反应,请计算:(1)生成氢气的质量(结果精确到0.1g).
(2)将(1)的结果标在图中;
(3)反应后所得溶液中溶质的质量分数(写出计算过程,结果精确到0.1%).
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)锌和稀硫酸反应生成硫酸锌和氢气,根据锌的质量可以计算生成氢气的质量;
(3)根据锌的质量可以计算生成硫酸锌的质量,进一步可以计算硫酸锌溶液中硫酸锌的质量分数.
(3)根据锌的质量可以计算生成硫酸锌的质量,进一步可以计算硫酸锌溶液中硫酸锌的质量分数.
解答:解:(1)设生成氢气的质量为x,生成硫酸锌的质量为y,
Zn+H2SO4═ZnSO4+H2↑,
65 161 2
13g y x
=
=
,
x=0.4g,y=32.2g,
答:生成氢气的质量是0.4g.
(2)生成氢气的质量如图中所示:

(3)反应后所得溶液中溶质的质量分数为:
×100%=28.6%,
答:反应后所得溶液中溶质的质量分数为28.6%.
Zn+H2SO4═ZnSO4+H2↑,
65 161 2
13g y x
| 65 |
| 13g |
| 161 |
| y |
| 2 |
| x |
x=0.4g,y=32.2g,
答:生成氢气的质量是0.4g.
(2)生成氢气的质量如图中所示:

(3)反应后所得溶液中溶质的质量分数为:
| 32.2g |
| 100g+13g-0.4g |
答:反应后所得溶液中溶质的质量分数为28.6%.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案
相关题目
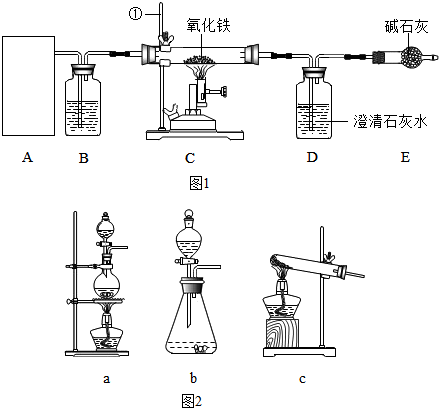

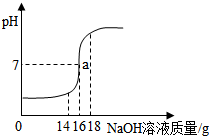 将5%的NaOH溶液逐滴加入到10g稀盐酸中,边加边搅拌,随着NaOH溶液的加入,溶液pH的变化如图所示.边回答:
将5%的NaOH溶液逐滴加入到10g稀盐酸中,边加边搅拌,随着NaOH溶液的加入,溶液pH的变化如图所示.边回答: 人体胃酸过多会引起胃病.如图所示为某抗酸药包装标签上的部分文字,请回答下列问题.
人体胃酸过多会引起胃病.如图所示为某抗酸药包装标签上的部分文字,请回答下列问题.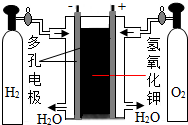 煤、石油、天然气等化石燃料是不可再生能源.植物在光照条件和叶绿素催化作用下发生的光合作用可产生比较丰富的可再生资源,其化学方程式为
煤、石油、天然气等化石燃料是不可再生能源.植物在光照条件和叶绿素催化作用下发生的光合作用可产生比较丰富的可再生资源,其化学方程式为
