题目内容
现有
A、B、C、D四种元素,核内质子数依次增大.A原子核内没有中子,B原子比A原子多两个电子层,且B最外层电子数比A多两个,C原子得到1个电子后核外有18个电子,D原子核内质子数比B原子核内质子数多5.则:(1)
写出A、B、C、D的名称和元素符号;(2)
画出A、B、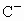 、D的结构示意图;
、D的结构示意图;
(3)D
单质的化学性质如何?为什么?
答案:略
解析:
解析:
|
答案: (1)A:氢H B:铝Al C:氯Cl D:氩Ar(2) (3)D 单质的化学性质稳定,很难与其他物质发生化学反应,因为D原子的最外层有8个电子,达到稳定结构.解析:根据题给条件得知: A、B、C、D四种元素核电荷数依次增大,A是无中子的元素,只有氢原子无中子,所以A是氢元素,B比A多两个电子层而且最外层比A多2个电子,根据核外电子排布知识确定B是铝元素;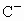 是阴离子,说明得到1个电子后有18个电子,那么C元素为氯元素,根据B元素进而推出D元素为氩元素. 是阴离子,说明得到1个电子后有18个电子,那么C元素为氯元素,根据B元素进而推出D元素为氩元素. |

练习册系列答案
 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案
相关题目
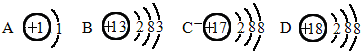
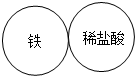 (2013?松北区二模)现有A、B、C、D四种物质分别是稀盐酸、氢氧化钠溶液、铁粉、硝酸银溶液,用四个圆形表示A(铁粉)、B(稀盐酸)、C(硝酸银溶液)、D(氢氧化钠溶液)四种物质,用相邻的圆形相切表示两种物质可以发生反应,请回答下列问题:
(2013?松北区二模)现有A、B、C、D四种物质分别是稀盐酸、氢氧化钠溶液、铁粉、硝酸银溶液,用四个圆形表示A(铁粉)、B(稀盐酸)、C(硝酸银溶液)、D(氢氧化钠溶液)四种物质,用相邻的圆形相切表示两种物质可以发生反应,请回答下列问题: