题目内容
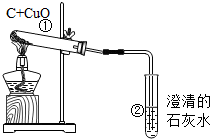
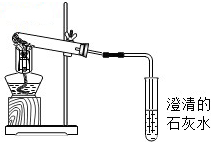 如图是木炭还原氧化铜的实验装置图:
如图是木炭还原氧化铜的实验装置图:(1)左侧试管中能观察到的现象为
(2)酒精灯加网罩的作用是
(3)写出碳在高温时还原氧化铜的化学方程式,并计算要使80g氧化铜完全还原,需要碳的质量至少是多少?(要求写出计算过程)
分析:(1)氧化铜为黑色,经还原后变成红色的铜,据此分析;
(2)酒精灯加网罩的作用是集中火焰,提高温度;
(3)碳在高温时还原氧化铜的化学方程式为C+2CuO
2Cu+CO2↑;
(2)酒精灯加网罩的作用是集中火焰,提高温度;
(3)碳在高温时还原氧化铜的化学方程式为C+2CuO
| ||
解答:解:(1)碳在高温时还原氧化铜,使黑色氧化铜变成红色铜,所以现象是黑色粉末变红;
(2)酒精灯加网罩的作用是集中火焰,提高温度;
(3)碳在高温时还原氧化铜的化学方程式是C+2CuO
2Cu+CO2↑;设还原80g氧化铜需碳x,则
C+2CuO
2Cu+CO2↑;
12 160
x 80
=
x=6g
答:还原80g氧化铜需碳6g.
故答案为:(1)黑色粉末变红;(2)提高温度;(3)C+2CuO
2Cu+CO2↑;6g.
(2)酒精灯加网罩的作用是集中火焰,提高温度;
(3)碳在高温时还原氧化铜的化学方程式是C+2CuO
| ||
C+2CuO
| ||
12 160
x 80
| 12 |
| 160 |
| x |
| 80g |
x=6g
答:还原80g氧化铜需碳6g.
故答案为:(1)黑色粉末变红;(2)提高温度;(3)C+2CuO
| ||
点评:本题主要考查木炭的化学性质和化学方程式的书写等方面的知识,书写化学方程式时要注意遵循质量守恒定律.计算过程要规范.

练习册系列答案
相关题目
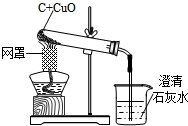 如图是木炭还原氧化铜的探究实验装置.
如图是木炭还原氧化铜的探究实验装置.【提出问题】木炭还原氧化铜产生什么气体?
【提出猜想】产生的气体有三种情况:
①CO;②CO2;③
【设计方案】实验前后分别对试管和烧杯里的物质进行称量,数据设计如下:
| 称量对象 | 反应前质量 | 反应后质量 | 质量差 |
| 试管+固体混合物 | M1 | M2 | △m1即( M1-M2) |
| 烧杯+澄清石灰水 | M3 | M4 | △m2即( M4-M3) |
(2)若猜想②正确,理论上△m1与△m2 的关系是:△m1
【实验并记录】实验得到的数据如下表:
| 称量对象 | 反应前质量 | 反应后质量 | 质量差 |
| 试管+固体混合物 | 69.8g | 65.4g | △m1 |
| 烧杯+澄清石灰水 | 118.8g | 122.6g | △m2 |
【反思与评价】经查阅资料知道:木炭还原氧化铜产生CO2气体,该反应的化学方程式为:
本次实验结果与资料显示不一致.对其可能原因有同学提出下列分析,其中合理的是
A.装置漏气 B.生成的CO2部分与过量的C反应生成了CO
C.澄清石灰水吸收CO2效果不好 D.装置内还有CO2气体未被吸收.
 如图是木炭还原氧化铜的实验.于实验前后对两个试管的物质进行称量,并检查了装置的气密性,肯定不漏气.
如图是木炭还原氧化铜的实验.于实验前后对两个试管的物质进行称量,并检查了装置的气密性,肯定不漏气.某次实验的数据如下:
| 反应前 | 反应后 | 质量差 | |
| 试管+固体混合物 | 65.8g | 61.4g | △m1 |
| 试管+石灰水 | 118.8g | 122.6g | △m2 |
(2)本次实验结果与理论值是否一致?答:
①
②
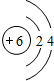 碳与碳的化合物在工农业生产及日常生活中有广泛的用途.
碳与碳的化合物在工农业生产及日常生活中有广泛的用途.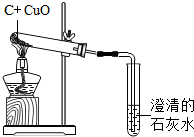
 如图是木炭还原氧化铜的实验:
如图是木炭还原氧化铜的实验: 碳与碳的化合物在工农业生产及日常生活中有广泛的用途.
碳与碳的化合物在工农业生产及日常生活中有广泛的用途. 是碳原子结构示意图,碳原子的质子数是
是碳原子结构示意图,碳原子的质子数是