题目内容
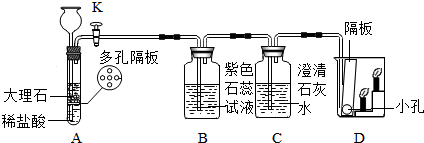
4.有一包白色粉末,可能是CuSO4、CaCO3、BaCl2、Na2SO4、KOH、KCl中的一种或几种,为证明其组成,进行如下实验: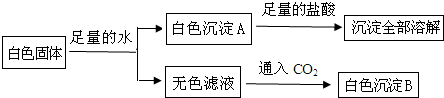
根据上述实验现象判断:
(1)白色沉淀A的化学式是CaCO3;
(2)白色固体中一定不含CuSO4、Na2SO4,一定含有CaCO3、BaCl2、KOH,可能含有KCl;
(3)写出通入CO2生成白色沉淀的化学方程式2KOH+CO2=K2CO3+H2O,K2CO3+BaCl2=BaCO3↓+2KCl.
分析 根据硫酸铜在溶液中显蓝色,碳酸钙难溶于水,碳酸钙会与酸反应生成二氧化碳气体,硫酸钡沉淀难溶于酸,二氧化碳会与碱反应生成盐和水,碳酸根离子会与钡离子生成白色的碳酸钡沉淀等知识进行分析解答.
解答 解:硫酸铜溶于水得到蓝色溶液,题中加入足量的水溶解后是无色的溶液,所以在白色固体中一定不含硫酸铜,同时能形成白色沉淀的有碳酸钙,硫酸钠和氯化钡也可以反应生成白色沉淀,而白色沉淀能全部溶于稀硝酸,硫酸钠和氯化钡反应生成的硫酸钡不溶于稀硝酸,所以白色沉淀A为碳酸钙,所以硫酸钠和氯化钡最多含有一种,向无色滤液中通入CO2气体,得到白色沉淀,通入二氧化碳后产生了白色沉淀,根据题中所给的物质分析,这种白色沉淀只能是碳酸钡,但是二氧化碳不能与氯化钡直接反应生成沉淀,从而我们判断还应该有氢氧化钾,氢氧化钾与二氧化碳反应生成碳酸钾后,碳酸钾与氯化钡反应生成了碳酸钡沉淀,所以原白色粉末中还含有物质的是氯化钡、氢氧化钾,而混合物中是否含有氯化钾对实验现象不会造成影响,所以:
(1)白色沉淀A的化学式是:CaCO3;
(2)白色固体中一定不含:CuSO4、Na2SO4,一定含有:CaCO3、BaCl2、KOH,可能含有KCl;
(3)通入CO2生成白色沉淀的反应是氢氧化钾和二氧化碳反应生成碳酸钾和水,碳酸钾和氯化钡反应生成白色的碳酸钡沉淀和氯化钾,化学方程式为:2KOH+CO2=K2CO3+H2O,K2CO3+BaCl2=BaCO3↓+2KCl.
故答案为:(1)CaCO3;
(2)CuSO4、Na2SO4,CaCO3、BaCl2、KOH,KCl;
(3)2KOH+CO2=K2CO3+H2O,K2CO3+BaCl2=BaCO3↓+2KCl.
点评 在解此类题时,首先分析题中所给物质的性质,然后依据题中的现象确定各种物质的存在性,最后确定混合物的成分.

| A. | 厨房煤气泄漏,立即打开排气扇电源 | |
| B. | 用软水洗衣服比用硬水洗效果好 | |
| C. | 防煤气中毒,煤炉上放 盆水 | |
| D. | 寻找一种催化剂将水变为汽油 |
【提出问题】铁与硫酸溶液反应生成的气体为什么有刺激性气味?
【查阅资料】
(1)6H2SO4(浓)+2Fe═Fe2(SO4)3+6H2O+3SO2↑
(2)SO2可使品红溶液的红色褪去
【进行猜想】铁与不同浓度的硫酸溶液反应,生成的气体产生可能有二氧化硫
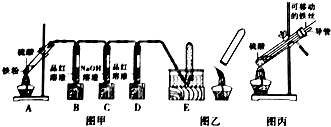
【实验探究】小明用图甲所示装置进行实验,并将E中收集到的气体进行如图乙所示的爆鸣实验.
请帮助小明完成如表:
| 实验现象 | |||||
| 硫酸溶液浓度 | B中品红溶液 | D中品红溶液 | 爆鸣实验 | A中生成气体成分 | |
| 实验一 | 98% | 褪色 | 不褪色 | 无爆鸣声 | 只有SO2 |
| 实验二 | 45% | 稍有褪色 | 不褪色 | 有爆鸣声 | SO2和H2 |
| 实验三 | 25% | 不褪色 | 不褪色 | 有爆鸣声 | 只有H2 |
【交流反思】
(1)写出实验三中铁与硫酸溶液反应的化学方程式Fe+H2SO4═FeSO4+H2↑,写出实验二中发生爆鸣反应的化学方程式2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O.
(2)实验一中C装置的作用是吸收二氧化硫.【拓展延伸】小明又将A装置进行了如图丙所示的改进,试分析:增加的导管下端伸入液
面以下原因形成液封,防止生成的气体逸出,该导管所起的作用是平衡试管内外的压强,防止橡皮塞飞出.
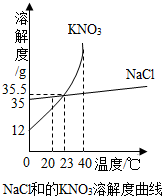
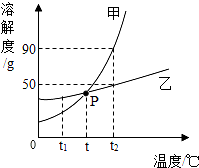 如图为甲、乙两种物质的溶解度曲线,据图回答下列问题.
如图为甲、乙两种物质的溶解度曲线,据图回答下列问题.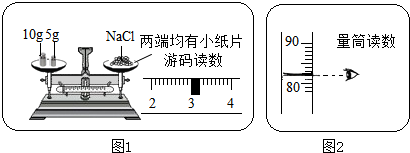
 用科学方法认识和改造物质
用科学方法认识和改造物质