题目内容
17.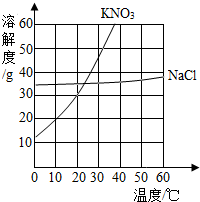 根据图中KNO3和NaCl的溶解度曲线,回答下列问题.
根据图中KNO3和NaCl的溶解度曲线,回答下列问题.(1)10℃时将20gKNO3完全溶解,至少需要水100g;
(2)将 20℃KNO3的不饱和溶液转变为饱和溶液,在保持溶质质量不变的条件下,可采用的方法有降温(或蒸发溶剂)(写一种即可);
(3)将40℃均含100g水的KNO3饱和溶液、NaCI饱和溶液降温至10℃析出晶题较多的是KNO3;
(4)提纯混有少量KNO3的NaCl,方法是蒸发溶剂(或蒸发结晶);
(5)若要配制100g,10%的KNO3溶液,需要40%的KNO3溶液25g.
分析 (1)据该温度下硝酸钾的溶解度分析解答;
(2)不饱和溶液变为饱和溶液的一般方法是加入溶质、降温或蒸发溶剂;
(3)据不同温度下硝酸钾的溶解度分析解答;
(4)据硝酸钾和氯化钠的溶解度随温度变化情况分析解答;
(5)据溶质的质量=溶液的质量×溶质的质量分数分析解答.
解答 解:(1)10℃时硝酸钾的溶解度是20g,即100g水中最多溶解20g的硝酸钾,所以将20gKNO3完全溶解,至少需要水100g;
(2)硝酸钾的溶解度随温度降低而减小,所以将20℃KNO3的不饱和溶液转变为饱和溶液,在保持溶质质量不变的条件下,可采用降温或蒸发溶剂恰好饱和的方法有;
(3)由图可知:40℃时硝酸钾的溶解度 远大于氯化钠的溶解度,因此该温度下均含100g水的KNO3饱和溶液、NaCI饱和溶液中含有溶质的质量大小是硝酸钾大于氯化钠,降温至10℃硝酸钾的溶解度变化比氯化钠大,故析出晶题较多;
(4)硝酸钾的溶解度受温度影响较大,氯化钠的溶解度受温度影响较小,所以提纯混有少量KNO3的NaCl,可采取蒸发溶剂或蒸发结晶的方法;
(5)若要配制100g,10%的KNO3溶液,需要硝酸钾的质量源于40%的KNO3溶液,故二者所含硝酸钾的质量相等;设需要40%的KNO3溶液的质量为x,则有:100g×10%=40%×x,解得x=25g;
故答案为:(1)100;(2)降温(或蒸发溶剂);(3)KNO3;(4)蒸发溶剂(或蒸发结晶);(5)25.
点评 本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了饱和溶液与不饱和溶液的相互转化、有关溶液和溶质质量分数的计算,解答时计算要准确.

练习册系列答案
相关题目
12. 如图为实验室制取氢气的发生装置,若液面刚好不与锌粒接触面又无酸液可加,要得到氢气且保证H2的量不受影响,可从长颈漏斗中加入适量试剂的一组是( )
如图为实验室制取氢气的发生装置,若液面刚好不与锌粒接触面又无酸液可加,要得到氢气且保证H2的量不受影响,可从长颈漏斗中加入适量试剂的一组是( )
①食盐水 ②氢氧化钠溶液 ③氯化钡溶液 ④碳酸钠溶液.
 如图为实验室制取氢气的发生装置,若液面刚好不与锌粒接触面又无酸液可加,要得到氢气且保证H2的量不受影响,可从长颈漏斗中加入适量试剂的一组是( )
如图为实验室制取氢气的发生装置,若液面刚好不与锌粒接触面又无酸液可加,要得到氢气且保证H2的量不受影响,可从长颈漏斗中加入适量试剂的一组是( )①食盐水 ②氢氧化钠溶液 ③氯化钡溶液 ④碳酸钠溶液.
| A. | ①② | B. | ②④ | C. | ①③ | D. | ①④ |
2.下列图示实验操作中,正确的是( )
| A. | 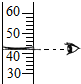 读液体体积 | B. | 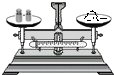 称量固体质量 | C. | 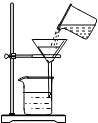 过滤 | D. | 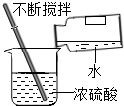 稀释浓硫酸 |
6.如图所示的实验中,得出的结论不正确的是( )
| A. | 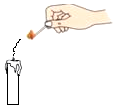 蜡烛刚熄灭时产生的白烟能燃烧,说明白烟具有可燃性 | |
| B. | 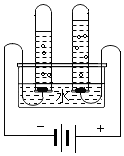 电解水实验能生成氮气和氧气,说明水是由氮元素和氧元素构成的 | |
| C. | 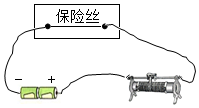 电流过大时,保险丝会自动熔断,说明此时通过保险丝的电流大于保险丝能承受的最大电流 | |
| D. | 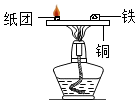 纸团燃烧而铁不燃烧,说明纸的着火点高于铁的着火点 |
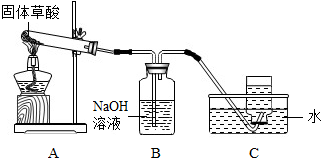
 A、B、C、D、E是初中常见的不同类别的物质.图中短线相连的物质间能相互发生反应. 已知A是常用于改良酸性土壤的碱,C是人体胃液的主要成分,E和C反应后生成浅绿色溶液;D是一种无色气体.B可能是碳酸钠;D在日常生活中的用途是灭火;写出工业冶炼E的化学方程式Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;写出A和B反应的化学方程式Ca(OH)2+Na2CO3=CaCO3↓+2NaOH.
A、B、C、D、E是初中常见的不同类别的物质.图中短线相连的物质间能相互发生反应. 已知A是常用于改良酸性土壤的碱,C是人体胃液的主要成分,E和C反应后生成浅绿色溶液;D是一种无色气体.B可能是碳酸钠;D在日常生活中的用途是灭火;写出工业冶炼E的化学方程式Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;写出A和B反应的化学方程式Ca(OH)2+Na2CO3=CaCO3↓+2NaOH. 如图是某化肥包装袋上的部分说明:
如图是某化肥包装袋上的部分说明: