题目内容
在A+CO2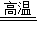 2B的反应中,已知4.4gCO2完全反应生成5.6gB.下列说法中错误的是( )
2B的反应中,已知4.4gCO2完全反应生成5.6gB.下列说法中错误的是( )A.参加反应的A的质量为1.2g
B.A的相对原子质量为12
C.B的相对分子质量是28
D.若4.4g CO2与2.4gA充分反应会生成6.8gB
【答案】分析:A、根据质量守恒定律分析;
B、根据化学方程式计算分析;
C、根据化学方程式计算分析;
D、根据质量守恒定律分析.
解答:解:A、已知4.4gCO2完全反应生成5.6gB,根据质量守恒定律可知,参加反应的A的质量为5.6g-4.4g=1.2g,故A说法正确;
B、设A的相对原子质量为x,
A+CO2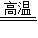 2B
2B
x 44
1.2g 4.4g
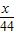 =
=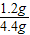 ,解得x=12,
,解得x=12,
因此A的相对原子质量为12,故B说法正确;
C、设B的相对分子质量是y,则
A+CO2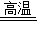 2B
2B
44 2y
4.4g 5.6g
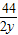 =
=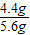 ,解得y=28
,解得y=28
因此B的相对原子质量为28,故C说法正确;
C、设与4.4g CO2反应的A的质量为z,则
A+CO2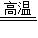 2B
2B
12 44
z 4.4g
 =
= ,解得z=1.2g
,解得z=1.2g
因此,根据质量守恒定律,若4.4g CO2与2.4gA充分反应会生成5.6gB.
故D.
点评:本题难度稍大,主要考查了质量守恒定律和化学方程式的计算.
B、根据化学方程式计算分析;
C、根据化学方程式计算分析;
D、根据质量守恒定律分析.
解答:解:A、已知4.4gCO2完全反应生成5.6gB,根据质量守恒定律可知,参加反应的A的质量为5.6g-4.4g=1.2g,故A说法正确;
B、设A的相对原子质量为x,
A+CO2
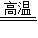 2B
2Bx 44
1.2g 4.4g
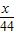 =
=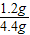 ,解得x=12,
,解得x=12,因此A的相对原子质量为12,故B说法正确;
C、设B的相对分子质量是y,则
A+CO2
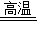 2B
2B44 2y
4.4g 5.6g
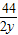 =
=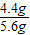 ,解得y=28
,解得y=28因此B的相对原子质量为28,故C说法正确;
C、设与4.4g CO2反应的A的质量为z,则
A+CO2
 2B
2B12 44
z 4.4g
 =
= ,解得z=1.2g
,解得z=1.2g因此,根据质量守恒定律,若4.4g CO2与2.4gA充分反应会生成5.6gB.
故D.
点评:本题难度稍大,主要考查了质量守恒定律和化学方程式的计算.

练习册系列答案
 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案
相关题目
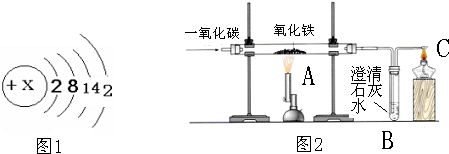
 ,试判断:
,试判断: 2B的反应中,已知4.4gCO2完全反应生成5.6gB.下列说法中错误的是
2B的反应中,已知4.4gCO2完全反应生成5.6gB.下列说法中错误的是