题目内容
16.埃博拉病毒是当今世界上最凶险的病毒之一,最近科学家研制出一种能抗击该病毒的药物,其化学式为C5H4N3O2F.下列有关这种药物的说法,正确的是( )| A. | C5H4N3O2F中含有1个氧分子 | B. | 碳、氢元素的质量比是5:4 | ||
| C. | 1个C5H4N3O2F由15个原子构成 | D. | 该药物是由多种元素组成的混合物 |
分析 A、根据C5H4N3O2F的微观构成进行分析判断.
B、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断.
C、根据C5H4N3O2F的微观构成进行分析判断.
D、该药物是由C5H4N3O2F一种物质组成的,据此进行分析判断.
解答 解:A、C5H4N3O2F是由C5H4N3O2F分子构成的,不含氧分子,故选项说法错误.
B、碳、氢元素的质量比是(12×5):(1×4)≠5:4,故选项说法错误.
C、C5H4N3O2F是由C5H4N3O2F分子构成的,1个C5H4N3O2F分子由15个原子构成,故选项说法正确.
D、该药物是由C5H4N3O2F一种物质组成的,属于纯净物,故选项说法错误.
故选:C.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.区分下列各组物质所用的两种方法都合理的是( )
| 选项 | 需要区分的物质 | 方法一 | 方法二 |
| A | 氧化铜和木炭粉 | 放入水中,观察是否溶解 | 取样,分别滴加稀盐酸 |
| B | 硝酸钾和硝酸铵 | 分别溶于水,测温度 | 取样,加熟石灰研磨 |
| C | 生铁和钢 | 取样,分别加入硫酸铜溶液 | 分别用磁铁吸引 |
| D | 白酒和白醋 | 闻气味 | 取样,滴加酚酞 |
| A. | A | B. | B | C. | C | D. | D |
7.下列物质露置于空气中,一段时间后质量减轻的是( )
| A. | 浓硫酸 | B. | 石灰石 | C. | 浓盐酸 | D. | 烧碱 |
1.下列粒子中,决定元素化学性质的是( )
| A. | 质子数 | B. | 最外层电子数 | C. | 电子数 | D. | 中子数 |
18.元素在自然界里分布并不均匀,地壳中含量的多少分析,最丰富的金属元素是( )
| A. | Fe | B. | Al | C. | O | D. | Si |
19.下列关于溶液的说法中正确的是( )
| A. | 水可以溶解任何物质 | |
| B. | 饱和溶液就是不能再溶解任何物质的溶液 | |
| C. | 溶质可以是固体,也可以是液体或气体 | |
| D. | 物质溶于水时都放出热量 |
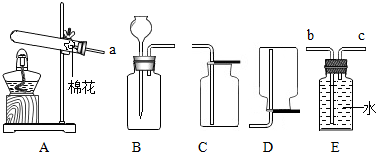
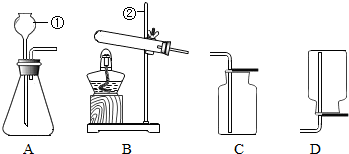 现有如图初中化学常用的制取气体部分装置.请完成以下各题:
现有如图初中化学常用的制取气体部分装置.请完成以下各题: