题目内容
13.小明同学发现卖气球的小贩将铝制易拉罐放入一个装有氢氧化钠溶液的罐子里,不一会儿就有氢气产生.回到学校,他在老师的指导下将10g金属铝与40g 氢氧化钠溶液放在烧杯中反应,至不再产生气体时,烧杯中仍有固体残余物(NaAlO2可溶于水),且烧杯内的物质总质量减少为49.7g.(1)根据定律,反应中产生的氢气质量为0.3g.
(2)所用氢氧化钠溶液中溶质的质量分数为多少?
(有关反应的化学方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑)
分析 (1)由2Al+2NaOH+2H2O=2NaAlO2+3H2↑,因此,使用质量守恒定律,可由反应前后质量差计算出生成氢气的质量;
(2)由反应放出氢气的质量,根据反应的化学方程式计算参加反应的氢氧化钠的质量.
解答 解:(1)根据质量守恒定律,恰好完全反应后生成氢气的质量=10g+40g-49.7g=0.3g;
(2)设所用氢氧化钠溶液中溶质的质量为x
2Al+2NaOH+2H2O=2NaAlO2+3H2↑,
80 6
x 0.3g
$\frac{80}{x}=\frac{6}{0.3g}$
x=4g
烧杯中仍有固体残余物,说明氢氧化钠溶液完全反应
所用氢氧化钠溶液中溶质的质量分数为$\frac{4g}{40g}×$100%=10%.
答案:
(1)0.3;
(2)所用氢氧化钠溶液中溶质的质量分数为10%.
点评 根据反应的化学方程式可以表示反应中各物质的质量比,由反应中任一物质的质量可计算出反应中其它物质的质量.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.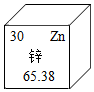 元素周期表中锌元素的某些信息如图所示,下列有关锌的说法不正确的是( )
元素周期表中锌元素的某些信息如图所示,下列有关锌的说法不正确的是( )
 元素周期表中锌元素的某些信息如图所示,下列有关锌的说法不正确的是( )
元素周期表中锌元素的某些信息如图所示,下列有关锌的说法不正确的是( )| A. | 原子核内有30个质子 | |
| B. | 是金属元素 | |
| C. | 相对原子质量为78.96g | |
| D. | 缺锌会引起食欲不振,生长迟缓,发育不良 |
4.下列实验进行中的现象或实验原理正确的是( )
| A. | 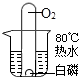 白磷始终不燃烧 | B. | 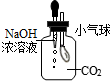 小气球变瘪 | ||
| C. | 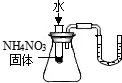 U形管内液面左高右低 | D. | 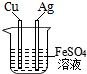 验证Fe,Cu,Ag的金属活性强弱 |
1.成语被誉为中华民族的瑰宝.下列成语中,其本意主要为化学变化的是( )
| A. | 磨杵成针 | B. | 木已成舟 | C. | 死灰复燃 | D. | 积土成山 |
18.下列关于实验现象的描述正确的是( )
| A. | 磷在氧气中燃烧,产生大量白色烟雾 | |
| B. | 木炭在氧气中燃烧,发出白色火焰,生成使澄清石灰水变浑浊的气体 | |
| C. | 镁带在空气中燃烧,发出耀眼的白光,放出大量的热,生成白色固体 | |
| D. | 蜡烛在空气中燃烧,发白光,放出大量的热 |
5.把稀硫酸、氢氧化钙溶液、氯化钠溶液和碳酸钾溶液四种物质两两混合,发生的复分解反应共有( )
| A. | 1个 | B. | 2个 | C. | 3个 | D. | 4个 |