题目内容
15.请根据如图所示实验回答下列问题: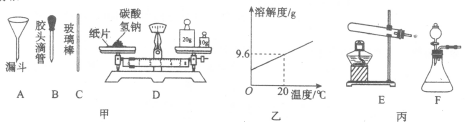
(1)图甲是配制碳酸氢钠溶液可能会用到的部分仪器.其中不需要的仪器是A(填序号),用图中所示方法称取一定量的碳酸氢钠固体,会导致所称取溶质的质量偏小(选填“偏大”“偏小”或“不变”).
(2)图乙所示是碳酸氢钠的溶解度曲线图.在室温(20℃)下,无法配制出质量分数为10%的碳酸氢钠溶液.请你通过计算说明:$\frac{9.6g}{100g+9.6g}×100%$≈8.8%<10%.
(3)图丙是实验室制取气体的发生装置.若实验室制取氧气:选用E装置,其反应原理可能是2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑(用化学方程式表示);选用F装置的药品为MnO2和H2O2.
分析 (1)根据配制溶液的操作和用托盘天平称量的方法分析回答;
(2)根据在室温时碳酸氢钠的溶解度分析计算;
(3)根据装置的特点选用药品制取氧气,写出反应的方程式.
解答 解:(1)称量碳酸氢钠用图中的托盘天平,溶解配制溶液时用了图中的胶头滴管和玻璃棒,用不到的仪器是漏斗;由图示可知,在称量碳酸氢钠时,左边有纸片,右边没有,则使称量的碳酸氢钠的质量偏小;,
(2)由碳酸氢钠的溶解度曲线图可知,在在室温(20℃)下,碳酸氢钠的溶解度是9.6g,所配置的溶液的最大溶质质量分数是:$\frac{9.6g}{100g+9.6g}×100%$≈8.8%<10%
(3)由实验室制取气体的发生装置可知.该装置是加热固体制取气体,若实验室制取氧气,由于试管口处没有一团面花,应用氯酸钾和二氧化锰制取氧气,反应的化学方程式是:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;若选用F装置制取氧气,属于固液常温下反应制取氧气,应选用的药品是:MnO2和 H2O2.
故答为:(1)A,偏小;(2)$\frac{9.6g}{100g+9.6g}×100%$≈8.8%<10%;(3)2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,H2O2.
点评 本题的综合性较强,涉及到了溶液配制的操作、有关溶解度和溶质质量分数的计算和根据装置选择药品制取气体的知识,但难度不大,属于课本中的基础知识,加强基础知识的学习,有利于解答本题.

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目
6.物质的性质决定物质的用途.下列物质的用途主要由其化学性质决定的是( )
| A. | 用活性炭净水 | B. | 用氧气抢救病人 | ||
| C. | 用石墨做铅笔芯 | D. | 压缩空气给轮胎充气 |
20.关于金属物品的使用正确的是( )
| A. | 铝合金门窗变旧变暗后用砂纸或钢丝球打磨 | |
| B. | 铁桶中加入硫酸铜溶液和石灰乳配制杀菌剂波尔多液 | |
| C. | 铁锅内的水垢用质量分数为18%的热盐酸长时间浸泡 | |
| D. | 校内用钢架制作的自行车防雨棚应定期喷涂油漆防锈 |
7.物质性质决定用途.下列说法错误的是( )
| A. | 氮气化学性质稳定,可用于食品保护气 | |
| B. | Ca(OH)2具有碱性,可用于改良酸性土壤 | |
| C. | 食醋具有酸性,可用于除去水壶中的水垢 | |
| D. | 甲醛能使蛋白质变性,可用于食用水产品防腐 |
4.某物质的着火点为 t℃,图中该物质燃烧得最旺的点是( )
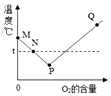

| A. | Q 点 | B. | N 点 | C. | P 点 | D. | M 点 |
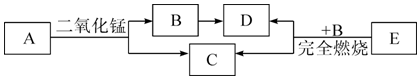
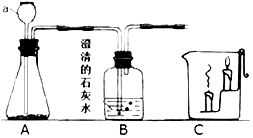 实验室有大理石、稀盐酸、棉花,相关仪器及用品:
实验室有大理石、稀盐酸、棉花,相关仪器及用品: