题目内容
3.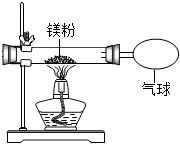 某兴趣小组甲为验证质量守恒定律,做了镁条在空气中燃烧的实验.
某兴趣小组甲为验证质量守恒定律,做了镁条在空气中燃烧的实验.(1)请写出镁条与氧气反应的化学方程式2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO;
(2)实验中发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵循质量守恒定律.我不同意该小组的观点,因为空气中的氧气参加了反应;
(3)小组乙按如图装置改进实验,却发现产物中还有少量黄色固体.
【提出问题】黄色固体是什么呢?
【査阅资料】①氧化镁为白色固体:
②镁能与氮气剧烈反应生成黄色的氮化镁(MgN2)固体:③氮化镁可与水剧烈反应产生氨气.氨气极易溶于水,溶液呈碱性.
【做出猜想】黄色固体是MgN2
【实验探究】请设计实验,验证猜想:
| 实验操作 | 实验现象及结论 |
| 1 取少量黄色固体于试管中,加入适量的水 ②滴加酚酞试液 | 现象:①产生有刺激性气味的气体 ②酚酞试液变红色 结论:证明猜想正确 |
分析 镁在空气中燃烧生成氧化镁;
显碱性的溶液能使酚酞试液变红色.
解答 解:(1)镁条与氧气反应生成氧化镁,反应的化学方程式为:2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO.
故填:2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO.
(2)因为空气中的氧气和镁反应生成了氧化镁,因此实验中发现燃烧产物的质量大于反应物镁条的质量.
故填:空气中的氧气参加了反应.
【实验探究】验证猜想如下表所示:
| 实验操作 | 实验现象及结论 |
| 1 取少量黄色固体于试管中,加入适量的水 ②滴加酚酞试液 | 现象:①产生有刺激性气味的气体 ②酚酞试液变红色 结论:证明猜想正确 |
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

练习册系列答案
相关题目
14.下列各组物质中按酸、碱、盐、氧化物的顺序排列的是( )
| A. | H2SO4、Na2O、MgCl2、Ca(OH)2 | B. | Na2CO3、Ba(OH)2、Na2O、H2SO4 | ||
| C. | HNO3、KOH、Na2CO3、CaO | D. | H2SO4、CaCO3、KOH、SO2 |
11. 元素周期表中铁元素的某些信息如图所示,下列有关铁的说法不正确的是( )
元素周期表中铁元素的某些信息如图所示,下列有关铁的说法不正确的是( )
 元素周期表中铁元素的某些信息如图所示,下列有关铁的说法不正确的是( )
元素周期表中铁元素的某些信息如图所示,下列有关铁的说法不正确的是( )| A. | 原子核内有26个质子 | B. | 相对原子质量为55.85 | ||
| C. | 是地壳中含量最多的金属元素 | D. | 是金属元素 |
18.在一个密闭容器中有X、Y、Z、Q四种物质,一定条件下充分反应,测得反应前后各物质的质量如表所示:
己知X和Q两种物质的相对分子质量均为M,下列推理中正确的足( )
| X | Y | Z | Q | |
| 反应前的质量/g | 8 | 10 | 1 | 21 |
| 反应后的质量/g | 0 | 21 | 待测 | 9 |
| A. | 反应后物质Z的质量为9g | |
| B. | 反应生成Y的质量为llg | |
| C. | 反应中物质Y与Q发生改变的质量之比为1:1 | |
| D. | 该反应的化学方程式中,物质X与Q的化学计量数之比为1:1 |
15.铁丝在氧气里燃烧后剩下来的球状物质中的成分是Fe3O4和少量铁,不含Fe2O3、Fe3O4和Fe2O3的分解温度,铁的熔点见表:下列有关说法错误的是( )
| Fe3O4 | Fe2O3 | 铁 | |
| 分解温度/℃ | 1538 | 1400 | / |
| 熔点/℃ | / | / | 1535 |
| A. | 铁丝在氧气里燃烧时产生火星四射现象 | |
| B. | 可以用稀盐酸验证球状物质中含有铁 | |
| C. | 铁丝燃烧时温度高于1400℃而低于1535℃ | |
| D. | Fe3O4中铁元素具有两种化合价 |
4.小明在网络中看到镁是航空工业的重要材料,欲通过实验探究镁的性质.
(1)小明查阅资料得知镁能与稀盐酸反应,该反应属于的基本反应类型是置换反应.
(2)他取一支试管,放入一根镁条,加入一定量硫酸铜溶液,观察到镁条表面有少量气泡产生,且有黑色物质生成.镁条与硫酸铜溶液反应的现象让小明感到困惑,他去图书馆查到相关资料:
资料1:硫酸铜溶液在配制时加入了少量硫酸;
资料2:当金属粉末颗粒很小时,容易成为黑色;
资料3:实验过程中发生了一系列复杂的反应,生成的黑色粉末可能是CuO、Cu中的一种或两种.
①镁条与硫酸铜溶液反应的实验中产生的气体可能为H2(填化学式).
②小明进一步设计实验确定黑色粉末的成分,请在下表中补全实验方案.
表中,结论I是黑色固体中含有CuO,实验一种固体与CO反应的化学方程式为CuO+CO$\frac{\underline{\;高温\;}}{\;}$Cu+CO2;现象I是样品质量增加.
(1)小明查阅资料得知镁能与稀盐酸反应,该反应属于的基本反应类型是置换反应.
(2)他取一支试管,放入一根镁条,加入一定量硫酸铜溶液,观察到镁条表面有少量气泡产生,且有黑色物质生成.镁条与硫酸铜溶液反应的现象让小明感到困惑,他去图书馆查到相关资料:
资料1:硫酸铜溶液在配制时加入了少量硫酸;
资料2:当金属粉末颗粒很小时,容易成为黑色;
资料3:实验过程中发生了一系列复杂的反应,生成的黑色粉末可能是CuO、Cu中的一种或两种.
①镁条与硫酸铜溶液反应的实验中产生的气体可能为H2(填化学式).
②小明进一步设计实验确定黑色粉末的成分,请在下表中补全实验方案.
| 实验操作 | 实验现象 | 结论 |
| 将黑色粉末过滤、晾干后,分成两份 | ||
| 将其中一份装入硬质玻璃管中,向其中通入CO后,加热,并将生成的气体通入澄清石灰水中 | 澄清石灰水 变浑浊 | 结论I |
| 将另一份置于坩埚中,称其质量为m1,在空气中加热一段时间后冷却,称其质量为m2. | 现象I | 黑色粉末中含Cu |