题目内容
5.氧气是我们身边常见的物质,以下有关氧气的叙述不正确的是( )| A. | 氧气具有可燃性 | B. | 氧气能提供动植物呼吸 | ||
| C. | 氧气能支持燃烧 | D. | 氧气的密度比空气稍大 |
分析 根据氧气的性质和用途分析判断,氧气的化学性质比较活泼,许多物质能与氧气发生化学反应,说明了氧气具有氧化性.氧气具有助燃性,但是氧气本身不能燃烧,不具有可燃性.氧气在通常状况下,是无色、无味的气体,密度比空气略大.
解答 解:
A、因为氧气具有助燃性,没有可燃性.故叙述错误;
B、氧气能供给动植物呼吸,故叙述正确;
C、因为氧气具有助燃性,所以氧气能支持燃烧.故叙述正确;
D、氧气在通常状况下,是无色、无味的气体,密度比空气略大,故叙述正确.
答案:A
点评 氧气是空气的主要成分之一,人们的日常生活离不开氧气,因为氧气能供给呼吸.支持燃烧是氧气的另一重要性质,绝大多数的物质燃烧离不开氧气,但氧气本身不具有可燃性,不能燃烧.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
15.下列化学反应中,属于复分解反应的是( )
| A. | Fe+CuSO4═FeSO4+Cu | B. | 2H2+O2 $\frac{\underline{\;点燃\;}}{\;}$ 2H2O | ||
| C. | CO2+H2O═H2CO3 | D. | NaOH+HCl═NaCl+H2O |
16.近年来有人提出了利用处理后的海水(主要成份是氯化钠溶液)吸收含二氧化硫的废气,该方法的流程如图所示.下列说法正确的是( )
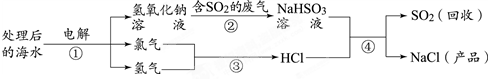

| A. | 反应中硫元素的化合价发生变化 | |
| B. | 反应①属于分解反应 | |
| C. | 反应③中,反应前后分子数目发生变化 | |
| D. | 反应④中,变化的离子是H+和HSO3- |
20.实验室有一瓶长期暴露在空气中的氢氧化钠固体样品,观察发现,样品表面有白色的粉末.某兴趣小组的同学对该样品的成分及含量进行了探究.
【提出问题1】该样品中含有哪些物质?
【提出猜想】通过分析,提出如下猜想:
猜想Ⅰ:已完全变质,该样品中只含Na2CO3;
猜想Ⅱ:部分变质,该样品中含有NaOH和Na2CO3.
则变质反应的化学方程式为2NaOH+CO2=Na2CO3+H2O.
【查阅资料】
①碱性的Na2CO3溶液可以与中性的CaCl2溶液发生复分解反应;
②CO2在饱和的碳酸氢钠溶液中几乎不溶解.
【实验探究1】为确定该样品的成分,小明设计了如下实验方案,请你一起完成下列实验报告.
【提出问题2】如何测量该部分变质样品中碳酸钠的质量分数?
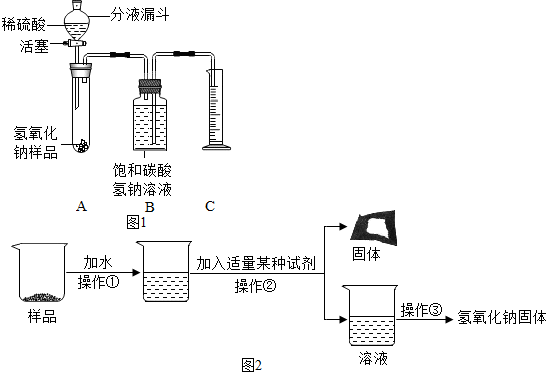
【实验探究2】小红同学设计如图1所示装置(铁架台略去),实验在27℃,101kPa下进行,步骤如下:①按图连接好装置;②用托盘天平准确称取该样品2.0g,放入A中试管内,向B中集气瓶中倒入饱和碳酸氢钠溶液至瓶颈处;③向分液漏斗中加入稀硫酸,打开活塞,让稀硫酸滴入试管中至过量,关闭活塞.反应结束后,量筒中收集到饱和碳酸氢氧化钠溶液220mL.请回答下列问题:
(1)在实验步骤①和②之间,还缺少一实验步骤,该实验步骤是检验装置的气密性;
(2)B中集气瓶盛装的饱和碳酸氢钠溶液不能用水代替,其理由是二氧化碳气体部分溶解在水中影响气体体积的测量;
(3)变质氢氧化钠样品中碳酸钠的质量分数为48%.(在27℃,101kPa时二氧化碳的密度为1.8g/L)(计算结果精确至1%)
【研究与讨论】小明同学认这小红的设计方案过于繁杂,他认为用托盘天平准确称取该样品2.0g后,只需要再称量装置A反应前的总质量(mA前)和完全反应后装置A的总质量(mA后),就能测量出该部分变质样品中碳酸钠的质量分数.
(1)小明认为反应中产生二氧化碳的质量等于mA前-mA后(填数学表达式),从而轻易的计算出该部分变质样品中碳酸钠的质量分数.
(2)小明计算出该部分变质样品中碳酸钠的质量分数的结果数据偏大,请你帮助他分析分析,原因可能是该反应过程中放热反应,导致一部分水以水蒸气的形式逸出.
【提出问题3】怎样提纯该样品得到纯净的氢氧化钠固体?
【实验探究3】为得到纯净的氢氧化钠固体,小亮设计了如图2所示的实验流程.
请回答下列问题:
(1)操作②中加入的适量某种试剂是氢氧化钙溶液(只写一种);
(2)最终所得氢氧化钠固体质量大于变质后样品中氢氧化钠的质量(填“小于”、“等于”或“大于”).
【实验反思】
实验探究1中的检验和实验探究3中的除杂都将碳酸钠进行了转化,但二者目的不同,请说出其中一个目的:将碳酸钠转化为碳酸钙,以免干扰氢氧化钠的检验.
【提出问题1】该样品中含有哪些物质?
【提出猜想】通过分析,提出如下猜想:
猜想Ⅰ:已完全变质,该样品中只含Na2CO3;
猜想Ⅱ:部分变质,该样品中含有NaOH和Na2CO3.
则变质反应的化学方程式为2NaOH+CO2=Na2CO3+H2O.
【查阅资料】
①碱性的Na2CO3溶液可以与中性的CaCl2溶液发生复分解反应;
②CO2在饱和的碳酸氢钠溶液中几乎不溶解.
【实验探究1】为确定该样品的成分,小明设计了如下实验方案,请你一起完成下列实验报告.
| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量样品溶于水,加入足量的氯化钙溶液; | 白色沉淀产生 | 该反应的化学方程式:CaCl2+Na2CO3=CaCO3↓+2NaCl |
| (2)将上述反应后的混合液过滤, 取滤液加入无色酚酞试液. | 酚酞试液变红色 | 证明猜想Ⅱ成立 |
【实验探究2】小红同学设计如图1所示装置(铁架台略去),实验在27℃,101kPa下进行,步骤如下:①按图连接好装置;②用托盘天平准确称取该样品2.0g,放入A中试管内,向B中集气瓶中倒入饱和碳酸氢钠溶液至瓶颈处;③向分液漏斗中加入稀硫酸,打开活塞,让稀硫酸滴入试管中至过量,关闭活塞.反应结束后,量筒中收集到饱和碳酸氢氧化钠溶液220mL.请回答下列问题:
(1)在实验步骤①和②之间,还缺少一实验步骤,该实验步骤是检验装置的气密性;
(2)B中集气瓶盛装的饱和碳酸氢钠溶液不能用水代替,其理由是二氧化碳气体部分溶解在水中影响气体体积的测量;

(3)变质氢氧化钠样品中碳酸钠的质量分数为48%.(在27℃,101kPa时二氧化碳的密度为1.8g/L)(计算结果精确至1%)
【研究与讨论】小明同学认这小红的设计方案过于繁杂,他认为用托盘天平准确称取该样品2.0g后,只需要再称量装置A反应前的总质量(mA前)和完全反应后装置A的总质量(mA后),就能测量出该部分变质样品中碳酸钠的质量分数.
(1)小明认为反应中产生二氧化碳的质量等于mA前-mA后(填数学表达式),从而轻易的计算出该部分变质样品中碳酸钠的质量分数.
(2)小明计算出该部分变质样品中碳酸钠的质量分数的结果数据偏大,请你帮助他分析分析,原因可能是该反应过程中放热反应,导致一部分水以水蒸气的形式逸出.
【提出问题3】怎样提纯该样品得到纯净的氢氧化钠固体?
【实验探究3】为得到纯净的氢氧化钠固体,小亮设计了如图2所示的实验流程.
请回答下列问题:
(1)操作②中加入的适量某种试剂是氢氧化钙溶液(只写一种);
(2)最终所得氢氧化钠固体质量大于变质后样品中氢氧化钠的质量(填“小于”、“等于”或“大于”).
【实验反思】
实验探究1中的检验和实验探究3中的除杂都将碳酸钠进行了转化,但二者目的不同,请说出其中一个目的:将碳酸钠转化为碳酸钙,以免干扰氢氧化钠的检验.
17.下列常见生活现象中,与其它变化不同的是( )
| A. | 冰雪融化 | B. | 榨取果汁 | ||
| C. | 点燃酒精加热火锅 | D. | 自行车轮胎爆炸 |