题目内容
17.现有部分变质的烧碱固体18.6g,与一定质量的溶质质量分数为14.6%的稀盐酸恰好完全反应,产生二氧化碳气体4.4g.请计算:(1)部分变质的烧碱固体中碳酸钠的质量是多少克?
(2)反应消耗稀盐酸溶液的总质量是多少克?
【反思与拓展】怎样除去烧碱溶液中的碳酸钠?(用化学方程式表示):Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
分析 (1)根据盐酸与碳酸钠反应的化学方程式和生成的二氧化碳的质量,列出比例式,就可计算出该样品中Na2CO3的质量;
(2)根据碳酸钠的质量求出氢氧化钠的质量,进而求出反应消耗稀盐酸溶液的总质量即可;
(3)根据碳酸钠和氢氧化钙反应生成氢氧化钠和碳酸钙沉淀进行解答.
解答 解:(1)设样品中碳酸钠的质量是x,消耗氯化氢的质量为y;
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 73 44
x y 4.4g
$\frac{106}{x}=\frac{73}{y}=\frac{44}{4.4g}$
解得:x=10.6g;y=7.3g;
(2)样品中氢氧化钠的质量为18.6g-10.6g=8g;
设氢氧化钠与盐酸反应消耗的氯化氢的质量为z;
NaOH+HCl═NaCl+H2O
40 36.5
8g z
$\frac{40}{8g}=\frac{36.5}{z}$
z=7.3g;
反应消耗稀盐酸溶液的总质量=$\frac{7.3g+7.3g}{144.6%}$=100g;
答:(1)样品中Na2CO3的质量为10.6g;(2)反应消耗稀盐酸溶液的总质量为100g;
(3)碳酸钠和氢氧化钙反应生成氢氧化钠和碳酸钙沉淀,所以可以用适量氢氧化钙溶液除去烧碱溶液中的碳酸钠,化学方程式为Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.故填:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
点评 在碱和盐的混合溶液中滴加盐酸时,盐酸首先与碱反应,然后再跟盐反应,所以在氢氧化钠和碳酸钠的混合物中滴加盐酸,一开始没有二氧化碳产生.

| A. | 纤维素是由C、H、O三种原子构成的 | |
| B. | 纤维素中C、H、O三种元素的原子数比为6:10:5 | |
| C. | 纤维素中C元素质量分数为$\frac{72}{162}$×100% | |
| D. | 纤维素属于有机物 |
| A. | 墙内开花墙外香 | |
| B. | 湿衣服经过晾晒变干 | |
| C. | 香水、汽油密闭保存 | |
| D. | 50mL酒精和50mL水混合后的体积小于100mL |
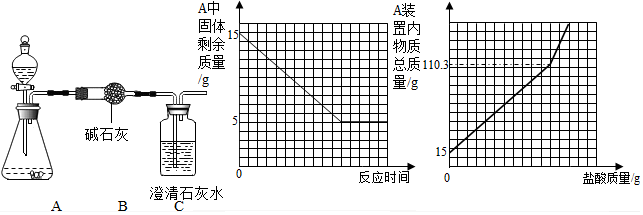

 某同学准备进行常见酸、碱、盐的性质实验时,发现实验台上有一瓶标签破损的溶液(如图),已知它是氯化钠溶液、氢氧化钠溶液、碳酸钠溶液三者中的一种,于是决定对这瓶溶液进行实验探究.
某同学准备进行常见酸、碱、盐的性质实验时,发现实验台上有一瓶标签破损的溶液(如图),已知它是氯化钠溶液、氢氧化钠溶液、碳酸钠溶液三者中的一种,于是决定对这瓶溶液进行实验探究.