题目内容
14.写出下列化学式所代表的物质名称:Cl2氯气;C碳;Fe3O4四氧化三铁;H2S硫化氢;Cu铜;H2SO4硫酸;CuSO4硫酸铜;NaCl氯化钠.
分析 化合物化学式的读法:一般是从右向左读,读作“某化某”,化学式中的下标表示构成这个分子的原子个数,有时不用读,有时为了区分不同价态的同种元素组成的化合物,需要读出化学式中的下角标,如SO2、P2O5等;据此进行分析解答
解答 解:Cl2是氯气的化学式;
C是碳单质的化学式;
根据氧化物的命名方法可知,Fe3O4读作四氧化三铁;
根据化合物的读法可知,H2S读作硫化氢;
Cu是金属单质铜的化学式;
H2SO4是硫酸的化学式;
根据化合物的化学式的读法可知,CuSO4读作硫酸铜;
根据化合物的命名方法可知,NaCl读作氯化钠.
故答案为:氯气;碳;四氧化三铁;硫化氢;铜;硫酸;硫酸铜;氯化钠.
点评 本题难度不大,掌握单质与化合物化学式的读法是正确解答此类题的关键.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
3.下列各个反应中,属于分解反应的是( )
| A. | 酒精+氧气$\stackrel{点燃}{→}$二氧化碳+水 | B. | 一氧化碳+氧气$\stackrel{点燃}{→}$二氧化碳 | ||
| C. | 碳酸氢铵$\stackrel{加热}{→}$氨气+二氧化碳+水 | D. | 乙炔+氧气$\stackrel{点燃}{→}$二氧化碳+水 |
2.玻璃瓶洗干净的标准是( )
| A. | 透明 | |
| B. | 内壁有少量水珠 | |
| C. | 内壁的水成股流下 | |
| D. | 内壁上附着的水既不聚成水滴,也不成股流下,均匀的形成水膜 |
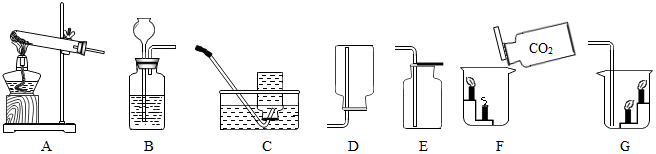
9.下列实验操作正确的是( )
| A. |  | B. |  | C. |  | D. |  |
6. 某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
(1)请写出镁条与氧气反应的化学方程式2Mg+O2 $\frac{\underline{\;点燃\;}}{\;}$2MgO.
(2)小明发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵循质量守恒定律.我不同意(“同意”或“不同意”)小明的观点,因为所有的化学反应都遵循质量守恒定律.
(3)小红按如图装置改进实验,验证了质量守恒定律,却发现产物中还有少量黄色固体.
【提出问题】黄色固体是什么呢?
【查阅资料】①氧化镁为白色固体;②镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2)固体;③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝.
【做出猜想】黄色固体是Mg3N2
【实验探究】请设计实验,验证猜想
【反思与交流】空气中N2的含量计远大于O2的含量,而镁条在空气中燃烧生成的MgO却远多于Mg3N2,为什么呢?请给出合理的解释氧气的化学性质比氮气更活泼,镁条更容易与氧气发生反应.
(4)该兴趣小组又做了镁条与盐溶液反应的实验,发现均能产生H2,实验现象如下:
上表中,用水进行实验的目的是对比.
根据上表中的实验现象,请写出三条结论,并分析可能的原因(不分析原因,不得分):①盐可以做镁与水反应的催化剂,因为盐能加快产生气体的速率;②温度改变反应速率,因为升高温度可以加快产生气体的速率;③高温度能使反应更复杂,因为升高温度使镁与水反应的生成物在与盐反应生成氨气(NH3).
 某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.(1)请写出镁条与氧气反应的化学方程式2Mg+O2 $\frac{\underline{\;点燃\;}}{\;}$2MgO.
(2)小明发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵循质量守恒定律.我不同意(“同意”或“不同意”)小明的观点,因为所有的化学反应都遵循质量守恒定律.
(3)小红按如图装置改进实验,验证了质量守恒定律,却发现产物中还有少量黄色固体.
【提出问题】黄色固体是什么呢?
【查阅资料】①氧化镁为白色固体;②镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2)固体;③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝.
【做出猜想】黄色固体是Mg3N2
【实验探究】请设计实验,验证猜想
| 实验操作 | 实验现象及结论 |
(4)该兴趣小组又做了镁条与盐溶液反应的实验,发现均能产生H2,实验现象如下:
| 实验序号 | 实验1 | 实验2 | 实验3 | |
| 与镁条反应的溶液 | NH4Cl | NaCl | Na2SO4 | H2O |
| 实验现象 | 有大量气泡产生 | 有较多气泡产生 | 有少量气泡产生 | 气泡极少 |
| 加热后,实验现象 | 气泡明显增多可闻到氨味 | 气泡增多 | 气泡增多 | 气泡增多 |
根据上表中的实验现象,请写出三条结论,并分析可能的原因(不分析原因,不得分):①盐可以做镁与水反应的催化剂,因为盐能加快产生气体的速率;②温度改变反应速率,因为升高温度可以加快产生气体的速率;③高温度能使反应更复杂,因为升高温度使镁与水反应的生成物在与盐反应生成氨气(NH3).