题目内容
9.某研究性学习小组为探究镁与水的反应,设计如下实验:步骤1:将镁条用砂纸打磨至光亮,分成两等份.
步骤2:将一份光亮的镁条置于冷水中,几乎没有观察到任何现象.
步骤3:将另一份光亮的镁条置于热水中,观察到有气泡产生.
(1)将镁条用砂纸打磨至光亮的原因是除去表面的氧化膜;
(2)经百度可知,活泼金属与水反应生成对应的碱和氢气,如果金属活动性越强,生成的碱的碱性越强.某同学就向步骤3的烧杯中滴加酚酞试液,观察到镁条的表面有明显的红色出现.请写出镁与热水反应的化学方程式:Mg+2H2O$\frac{\underline{\;\;△\;\;}}{\;}$Mg(OH)2↓+H2↑;
(3)步骤2和3对比可知,影响镁与水的反应速率的一个因素是温度;
(4)根据以上信息,若将金属钠加到硫酸铜溶液中,可能观察到的现象是有气体产生,溶液中产生蓝色沉淀.
分析 (1)根据金属镁能被空气中的氧气氧化生成氧化镁进行解答;
(2)根据镁条和热水反应生成氢氧化镁和氢气进行解答;
(3)根据步骤2和3对比可知,二者的不同之处在于温度不同进行解答;
(4)根据金属钠的活动性大于金属镁,所以将金属钠加到硫酸铜溶液中,金属钠要先与水反应生成氢氧化钠和氢气,氢氧化钠溶液和硫酸铜溶液反应生成氢氧化铜蓝色沉淀和硫酸钠进行解答.
解答 解:(1)金属镁能被空气中的氧气氧化生成氧化镁,所以将镁条用砂纸打磨至光亮的原因是:除去表面的氧化膜;故填:除去表面的氧化膜;
(2)镁条和热水反应生成氢氧化镁和氢气,该反应的化学方程式为Mg+2H2O$\frac{\underline{\;\;△\;\;}}{\;}$Mg(OH)2↓+H2↑;故填:Mg+2H2O$\frac{\underline{\;\;△\;\;}}{\;}$Mg(OH)2↓+H2↑;
(3)根据步骤2和3对比可知,二者的不同之处在于温度不同,所以步骤2和3对比可知,影响镁与水反应速率的因素是温度;故填:温度;
(4)金属钠的活动性大于金属镁,所以将金属钠加到硫酸铜溶液中,金属钠要先与水反应生成氢氧化钠和氢气,氢氧化钠溶液和硫酸铜溶液反应生成氢氧化铜蓝色沉淀和硫酸钠,故若将金属钠加到硫酸铜溶液中,推测可能观察到的现象是有气体产生,溶液中产生蓝色沉淀.故填:有气体产生,溶液中产生蓝色沉淀.
点评 在解此类题时,要结合金属活动性顺序来思考问题,一般可以通过金属被氧化的速度、与酸反应的剧烈程度、是否与相应的盐溶液反应三个方面来判断金属的活动性强弱.

练习册系列答案
相关题目
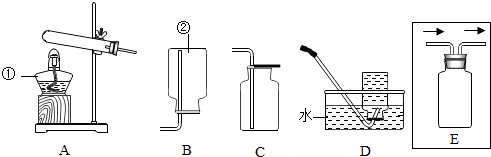
20.用下图所示实验装置进行相应实验,不能达到实验目的是( )
| A. |  收集氢气 | |
| B. |  验证二氧化碳的密度大于空气 | |
| C. | 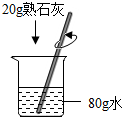 配制20%的溶液 | |
| D. |  向左推动针筒活塞可检验该装置的气密性 |
1.科学实验中、准确地分析实验数据是得到科学结论的保证.下列4个图象,能正确反映对应关系的是( )
| A. |  常温下,稀释KOH溶液 | |
| B. |  甲烷和过量的氧气在密闭容器中完全反应 | |
| C. | 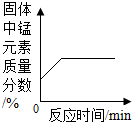 加热一定质量高锰酸钾固体 | |
| D. |  在装有稀硫酸的小烧杯中,不断慢慢滴加10%的Ba(OH)2溶液至过量 |
18.下列关于化学中“一定”的说法完全正确的一组是( )
| A. | 分子一定由原子构成;原子核一定由质子和中子构成 | |
| B. | 碱中一定含有氢元素;有机物中一定含有碳元素 | |
| C. | 纯净物一定由同种分子构成;生成盐和水的反应一定是中和反应 | |
| D. | 冷却热饱和溶液一定会有晶体析出;溶液中的溶剂一定是水 |
19. 探究影响化学反应速率的因素
探究影响化学反应速率的因素
(1)发现和提出问题
镁在空气中能够剧烈燃烧,铁丝在氧气中能够剧烈燃烧,而真金不怕火炼,这说明决定物质之间能否发生反应以及反应速率的内因是反应物本身的性质.
蜡烛在氧气中燃烧比在空气中燃烧剧烈,这一事例中影响化学反应速率的因素是氧气的浓度;夏天,将食品放在冰箱里不容易变质,这一事例说明温度也能影响化学反应速率,温度如何影响反应速率呢?
(2)猜想与假设
温度越高,反应速率越快
(3)收集证据
实验药品:颗粒大小相同的锌粒;两份相同溶质质量分数.不同温度的稀硫酸(20℃、40℃)
供选仪器:药匙、气体发生装置2套(气密性良好)、量筒2支、分液漏斗、秒表、胶头滴管、水槽、大试管2支.利用上述仪器和药品,补充完成下表的实验报告.
该实验可以观察或测量的量有多种,除了上述观测点外,可以观察或测量的量还有(写一条)相同时间内收集气体的体积(或反应结束所需的时间或消耗等量的锌粒所需的时间或消耗等量的稀硫酸所需的时间)等.
(4)结论与解释
从微观的角度分析“温度越高,反应速率越快”的原因是温度升高,粒子的运动的速率加快,有效碰撞机会增加.
(5)拓展分析
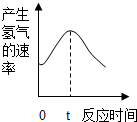
根据其他测定方位,实验小组的同学绘制了锌粒与稀硫酸反应产生氢气的速率随时间变化的曲线,如图所示,请据图分析:时间0-t内,反应速率逐渐加快的主要原因是锌与稀硫酸反应放热,温度升高,反应速率加快,时间t以后,反应速率逐渐减慢的主要原因是随着反应的进行,反应物的浓度越来越小,反应速率减慢.
 探究影响化学反应速率的因素
探究影响化学反应速率的因素(1)发现和提出问题
镁在空气中能够剧烈燃烧,铁丝在氧气中能够剧烈燃烧,而真金不怕火炼,这说明决定物质之间能否发生反应以及反应速率的内因是反应物本身的性质.
蜡烛在氧气中燃烧比在空气中燃烧剧烈,这一事例中影响化学反应速率的因素是氧气的浓度;夏天,将食品放在冰箱里不容易变质,这一事例说明温度也能影响化学反应速率,温度如何影响反应速率呢?
(2)猜想与假设
温度越高,反应速率越快
(3)收集证据
实验药品:颗粒大小相同的锌粒;两份相同溶质质量分数.不同温度的稀硫酸(20℃、40℃)
供选仪器:药匙、气体发生装置2套(气密性良好)、量筒2支、分液漏斗、秒表、胶头滴管、水槽、大试管2支.利用上述仪器和药品,补充完成下表的实验报告.
| 观察或测量的量 | 选用的仪器 | 实验步骤 | 实验现象 | 实验结论 |
| 产生相同体积(一试管)的气体所需时间 | 气体发生装置、秒表、胶头滴管、水槽、大试管、 药匙、量筒 | 温度越高,反应速率越快.反应的化学方程式是Zn+H2SO4═ZnSO4+H2↑ |
(4)结论与解释
从微观的角度分析“温度越高,反应速率越快”的原因是温度升高,粒子的运动的速率加快,有效碰撞机会增加.
(5)拓展分析
根据其他测定方位,实验小组的同学绘制了锌粒与稀硫酸反应产生氢气的速率随时间变化的曲线,如图所示,请据图分析:时间0-t内,反应速率逐渐加快的主要原因是锌与稀硫酸反应放热,温度升高,反应速率加快,时间t以后,反应速率逐渐减慢的主要原因是随着反应的进行,反应物的浓度越来越小,反应速率减慢.
 水是生命之源,我们应该了解水、爱护水.
水是生命之源,我们应该了解水、爱护水. 2015年12月,某餐厅发生一起爆炸事故,现场伴有大量浓烟冒出,距离事故发生地一千米左右,还能闻到浓浓的刺鼻味.消防部门第一时间赶到现场,扑灭大火,减少了人员伤亡和财产损失.根据要求回答问题:
2015年12月,某餐厅发生一起爆炸事故,现场伴有大量浓烟冒出,距离事故发生地一千米左右,还能闻到浓浓的刺鼻味.消防部门第一时间赶到现场,扑灭大火,减少了人员伤亡和财产损失.根据要求回答问题: