题目内容
6.某实验小组在研究酸的化学性质时,做了下列所示5个实验.(1)实验后,某试管中溶液呈浅绿色,该试管中发生反应的化学方程式为2HCl+Fe=FeCl2+H2↑.
(2)实验后,向某试管中滴加无色酚酞,溶液变红,再向此试管中加稀盐酸,只观察到溶液由红色变为无色.据此推断,该试管中最初发生的反应的化学方程式可能为NaOH+HCl=NaCl+H2O,2HCl+Ca(OH)2═CaCl2+2H2O(写出一个即可).
(3)将(2)反应后的溶液,与上述五支试管中某试管反应后的溶液混合,看到先产生气体,后出现沉淀.则混合前两试管溶液中,溶质分别为CaCl2HCl,Na2CO3NaCl;混合后溶液中溶质可能为NaCl(或CaCl2、NaCl,或(NaCl、Na2CO3)(写出一种即可).
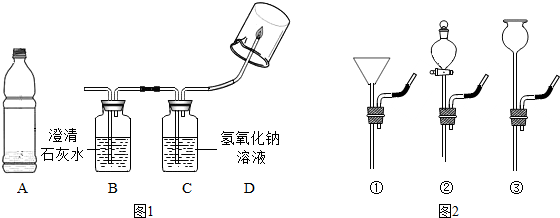
(4)科学实验提倡绿色环保,对实验装置进行微型化改进是一条很好的途径.如图甲是实验时制取并检验CO2的装置,图乙是对图甲实验装置微型化改进后的装置.

①图乙中微型塑料滴管在实验中的作用与图甲中的A(填字母编号)仪器相同;
②通常用甲装置完成该实验需要的盐酸是微型实验装置用量的10倍,采用微型实验装置具有的优点是药品用量少,产生的废弃物也少,方便操作;
③用乙装置完成“制取并验证CO2”的实验,消耗了0.73g 10%的盐酸,则实验过程中最多产生沉淀的质量是0.1g.
分析 (1)铁与盐酸反应生成的氯化亚铁溶液是浅绿色的,据此分析解答;
(2)向某试管中滴加无色酚酞,溶液变红,说明溶液显碱性,据此分析判断;
(3)将(2)反应后的溶液,与上述五支试管中某试管反应后的溶液混合,看到先产生气体,后出现沉淀;盐酸与碳酸盐反应生成气体,五支试管中可能形成的沉淀是碳酸钙;从而说明(2)反应后的溶液中含有盐酸、氯化钙,与之混合的溶液中含有碳酸根离子,碳酸盐过量,碳酸钙不溶于水,碳酸钠易溶于水,则说明是碳酸钠溶液与盐酸反应后的试管与实验(2)反应后的溶液混合,且碳酸钠过量,则该试管中的溶质是氯化钠、碳酸钠;
混合时因为先出现气体,后出现沉淀,说明溶液中盐酸反应完毕,故溶质中不会再有盐酸;混合后溶液中氯化钙与碳酸钠若恰好反应,则溶质只有氯化钠,若碳酸钠过量,则溶质是碳酸钠、氯化钠,若氯化钙过量,则溶质是氯化钙、氯化钠.
(4)①根据图乙中微型塑料滴管在实验中的作用与图甲中的分液漏斗仪器相同进行解答;
②根据采用“微型”实验装置具有的优点是药品用量少,产生的废弃物也少,方便操作进行解答;
③根据化学方程式中使用的氯化氢质量可求得二氧化碳的质量,进而求出沉淀的质量.
解答 解:(1)铁与盐酸反应生成的氯化亚铁溶液是浅绿色的,因此实验后,某试管中溶液呈浅绿色,说明该试管中发生反应的化学反应是铁和盐酸反应生成氯化亚铁和氢气;故填:2HCl+Fe=FeCl2+H2↑;
(2)向某试管中滴加无色酚酞,溶液变红,说明溶液显碱性,且该碱性物质过量,图示实验中碳酸钠、氢氧化钠、氢氧化钙溶液均显碱性,均有可能;再向此试管中加稀盐酸,只观察到溶液由红色变为无色,说明溶液中一定不是碳酸钠,因为碳酸钠与稀盐酸反应还会生成气体,故可能是氢氧化钠和盐酸反应生成氯化钠和水,氢氧化钙和盐酸反应生成氯化钙和水,方程式分别是:NaOH+HCl=NaCl+H2O,2HCl+Ca(OH)2═CaCl2+2H2O;故填:NaOH+HCl=NaCl+H2O,2HCl+Ca(OH)2═CaCl2+2H2O;
(3)将(2)反应后的溶液,与上述五支试管中某试管反应后的溶液混合,看到先产生气体,后出现沉淀;盐酸与碳酸盐反应生成气体,五支试管中可能形成的沉淀是碳酸钙;从而说明(2)反应后的溶液中含有盐酸、氯化钙,与之混合的溶液中含有碳酸根离子,碳酸盐过量,碳酸钙不溶于水,碳酸钠易溶于水,则说明是碳酸钠溶液与盐酸反应后的试管与实验(2)反应后的溶液混合,且碳酸钠过量,则该试管中的溶质是氯化钠、碳酸钠;混合时因为先出现气体,后出现沉淀,说明溶液中盐酸反应完毕,故溶质中不会再有盐酸;混合后溶液中氯化钙与碳酸钠若恰好反应,则溶质只有氯化钠,若碳酸钠过量,则溶质是碳酸钠、氯化钠,若氯化钙过量,则溶质是氯化钙、氯化钠;
故填:CaCl2 HCl;Na2CO3 NaCl;NaCl(或CaCl2、Na Cl,或(NaCl、Na2CO3);
(4)①图乙中微型塑料滴管在实验中的作用与图甲中的分液漏斗仪器相同,故填:A;
②采用“微型”实验装置具有的优点是药品用量少,产生的废弃物也少,方便操作,
故填:药品用量少,产生的废弃物也少,方便操作;
③设生成二氧化碳的质量为x.
CaC03+2HCl═CaCl2+H20+C02↑
73 44
0.73g×10% x
则 $\frac{73}{44}=\frac{0.73g×10%}{x}$,解得x=0.044g.
设生成沉淀的质量为y
Ca(OH)2+CO2═CaCO3↓+H2O
44 100
0.044g y
$\frac{44}{100}=\frac{0.044g}{y}$
y=0.1g
故填:0.1.
点评 本题以实验探究的形式考查了酸、碱、盐的相关化学性质,同时明确了物质反应时生成物溶液中溶质的判断方法,可从恰好反应或过量进行分析.

 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案| A. | 分子比原子大 | B. | 原子是实心球体 | ||
| C. | 分子之间有空隙而原子没有 | D. | 原子的质量主要集中在原子核上 |
| A. | 甲烷、二氧化碳、氢气 | B. | 二氧化碳、氯化氢、氮气 | ||
| C. | 二氧化硫、一氧化碳、二氧化氮 | D. | 氯化氢、氮气、氧气 |
| A. | 作为反应物 | B. | 使生成物质量增加 | ||
| C. | 改变化学反应速率 | D. | 减慢化学反应速率 |