题目内容
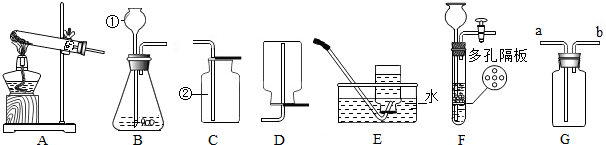
8.A、B、C三个烧杯中分别装有等质量的水,在t1℃时,向A烧杯中分别加入25g甲物质,向B、C两个烧杯中分别加入25g、15g乙物质,充分溶解后静置,现象如图所示,请回答下列问题:
(1)C烧杯中一定是不饱和溶液.
(2)右图是甲、乙两种物质的溶解度曲线,则曲线x是甲物质(填“甲”或“乙”),若将温度从t2℃降到t1℃时,A烧杯中的甲物质部分(填“全部”或“部分”)溶解,此时液溶是饱和溶液(填“饱和”或“不饱和”).
(3)若将甲、乙两种物质的混合物分离,所采用的方法最好是降温结晶.
分析 (1)根据饱和溶液的判断方法来分析;
(2)根据t1℃时两物质的溶解度大小来分析;根据物质溶解度受温度的影响来分析;
(3)据物质的溶解度随温度变化情况分析提纯物质的方法.
解答 解:(1)由题干可知,充分搅拌后A烧杯中还有不溶解的晶体存在,所以该烧杯中的溶液一定是饱和的,B中加入25g乙物质,搅拌后完全溶解,此溶液可能是不饱和的,也可能恰好是饱和状态,而同样多的水中,加入15g乙物质所得溶液一定是不饱和的,故填:C;
(2)有题干信息可知,t1℃时,乙物质的溶解度大于甲物质的溶解度,所以曲线x表示甲物质;若将温度从t2℃降到t1℃时,A烧杯中的甲物质仍不能完全溶解,此时的溶液仍为该温度下的饱和溶液;故填:部分;饱和;
(3)A的溶解度随温度的升高变化大,B的溶解度受温度影响不大,所以若甲物质中混有少量的乙物质,若要分离A、B两种物质,采用的最好方法是降温结晶.故填:降温结晶.
点评 本题难度不大,主要考查了固体溶解度曲线所表示的意义,通过本题可以加强学生对固体溶解度的理解,培养学生应用知识解决问题的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
8.下列物质中,属于氧化物的是( )
| A. | 03 | B. | Cu(OH)2 | C. | CaO | D. | NH4NO3 |
9.在一定条件下,一个密闭容器内发生某反应,测得反应前后各物质的质量如下表所示.下列有关说法不正确的是( )
| 物质 | a | b | c | d |
| 反应前的质量/g | 30 | 20 | 10 | 15 |
| 反应后的质量/g | X | y | 0 | 10 |
| A. | 参加反应的c与d的质量比为2:1 | B. | x的取值范围:0≤x≤30 | ||
| C. | 当y≤20时,该反应一定是化合反应 | D. | x+y=65 |
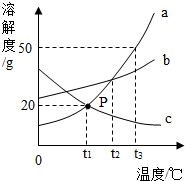 如图是a、b、c三种物质(均不含结晶水)的溶解度曲线,请填空:
如图是a、b、c三种物质(均不含结晶水)的溶解度曲线,请填空: