题目内容
4.早在春秋战国时期,我国就开始生产和使用铁器.某化学兴趣小组利用下图装置进行实验室模拟炼铁,请按要求填空:
(1)实验中观察到的现象是红棕色变成黑色,石灰水变浑浊(答2点);写出A中反应的化学方程式3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;B中反应的化学方程式Ca(OH)2+CO2=CaCO3↓+H2O.
(2)右边导气管口放置点燃的酒精灯的目的是燃烧多余的CO.
(3)当Fe2O3反应完全后,应先熄灭酒精喷灯(填“酒精喷灯”或“酒精灯”).
(4)澄清石灰水的作用检验生成物有二氧化碳生成.
(5)检测A中的产物是否为铁的化学方法是取样,在A中的产物中滴加稀硫酸,如果产生气泡,则含有铁(写出操作、现象、结论).
分析 (1)根据反应物生成物的性质分析反应的现象,根据CO还原Fe2O3的反应写出反应的方程式;根据二氧化碳能与氢氧化钙的反应,分析盛澄清石灰水的试管中可观察到的现象;
(2)根据一氧化碳有毒能污染空气,分析右边导气管口放置点燃的酒精灯的目的;
(3)根基实验的过程和注意的事项分析;
(4)根据二氧化碳和氢氧化钙反应会生成碳酸钙沉淀进行分析;
(5)根据铁和稀硫酸反应会生成硫酸亚铁和氢气进行分析.
解答 解:(1)在高温条件下,一氧化碳能与氧化铁反应生成了铁和二氧化碳.所以,A中观察到的现象是红棕色变成黑色;化学方程式是:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;B中二氧化碳能与氢氧化钙反应生成了碳酸钙沉淀和水,实验中盛澄清石灰水的试管中可观察到的现象是:石灰水变浑浊,化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O
(2)由于尾气中含有一氧化碳气体,能污染空气.所以右边导气管口放置点燃的酒精灯的目的是:燃烧多余的CO;
(3)当Fe2O3反应完全后,应先熄灭酒精喷灯,继续通一氧化碳直到装置中的固体冷却.实验结束时还需要继续通CO直至固体冷却,这是为了防止灼热的铁被进入的空气氧化;
(4)二氧化碳和氢氧化钙反应会生成碳酸钙沉淀,所以澄清石灰水的作用是:检验生成物有二氧化碳生成;
(5)取样,在A中的产物中滴加稀硫酸,如果产生气泡,则含有铁.
故答案为:(1)红棕色变成黑色,石灰水变浑浊;3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;Ca(OH)2+CO2=CaCO3↓+H2O;
(2)燃烧多余的CO;
(3)酒精喷灯;
(4)检验生成物有二氧化碳生成;
(5)取样,在A中的产物中滴加稀硫酸,如果产生气泡,则含有铁.
点评 本题主要考查了一氧化碳与氧化铁反应的现象、一氧化碳的性质、对大气的污染等知识,难度不大,属于基础性的练习题.

 一课一练课时达标系列答案
一课一练课时达标系列答案| A. | 与外焰接触部分被烧黑 | B. | 均匀的变黑 | ||
| C. | 与内焰接触部分被烧黑 | D. | 与焰心接触部分被烧黑 |
| A. | 碳+氧气 $\stackrel{点燃}{→}$ 二氧化碳 | B. | 石蜡+氧气 $\stackrel{点燃}{→}$ 二氧化碳+水 | ||
| C. | 氧化汞$\stackrel{加热}{→}$氧气+汞 | D. | 锌+稀盐酸→氯化锌+氢气 |

请根据各实验现象,帮助小王同学完成下列实验报告:
| 步骤 | 设计意图 | 实验现象 | 实验结论 |
| 实验1 | 燃烧与物质的关系 | 木条燃烧而玻璃棒不燃烧 | 可燃物才能燃烧 |
| 实验2 | 燃烧与氧气的关系 | 玻璃杯内蜡烛熄灭,外面的仍燃烧 | 说明燃烧还需要氧气 |
| 实验3 | 燃烧与温度的关系 | 小木条很快燃烧,小煤块很久才燃烧 | 燃烧还需要温度达到可燃物的着火点 |
(3)碳是人类接触最早、利用最多的元素之一.
①在元素周期表中,碳元素的信息如图
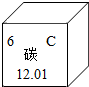 所示,碳元素的核内质子数目为6.
所示,碳元素的核内质子数目为6.②将碳粉与氧化铜混合后加强热,发生反应的化学方程式为C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑,该反应中碳表现出还原(填“氧化”或“还原”)性.
③下列用途中,主要利用了物质的物理性质的是ABD(填序号).
A干冰用于人工降雨 B将石墨用于制作电极
C一氧化碳用作气体燃料 D将小块金刚石镶在玻璃刀头上用来裁玻璃
④液态二氧化碳灭火器可用于扑救档案资料室发生的火灾,下列说法正确的是AB.
A.液态二氧化碳汽化后不会污染档案资料
B.二氧化碳可覆盖在燃烧物表面,隔绝空气
C.液态二氧化碳汽化时吸热,降低了可燃物的着火点
⑤石灰石用途非常广泛.可用来吸收火力发电厂煤燃烧时产生的二氧化硫废气,反应的化学方程式为:2CaCO3+2SO2+O2$\frac{\underline{\;高温\;}}{\;}$2CaSO4+2Y,Y的化学式为CO2.
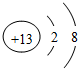 是某粒子的结构示意图,下列叙述错误的是( )
是某粒子的结构示意图,下列叙述错误的是( )| A. | 该元素的原子可直接构成物质 | B. | 该粒子具有稳定结构 | ||
| C. | 该元素原子的核外共有3个电子层 | D. | 该粒子是阴离子 |
| A. | 糯米酿酒 | B. | 车胎爆炸 | C. | 灯泡发光 | D. | 酒精挥发 |
| 实验步骤 | 实验现象 |
| ①取一定量的合金粉末,加入过量的氢氧化钠溶液,充分反应后过滤,滤纸上剩余物备用 | 粉末部分溶解,并有无色体放出 |
| ②取步骤①所得固体物质,加入过量的稀硫酸,充分反应 | 固体物质部分溶解,并有无色气体放出,溶液呈浅绿色 |
(1)该合金的组成是Al、Fe、Cu.
(2)①中发生反应的化学方程式为2Al+2H2O+2NaOH═2NaAlO2+3H2↑.
(3)②中发生反应的化学方程式为Fe+H2SO4═FeSO4+H2↑.
 如图是小明向试管中倾注液体的操作示意图,请你为小明任意指出两处错误:
如图是小明向试管中倾注液体的操作示意图,请你为小明任意指出两处错误: