题目内容
【题目】2016年10月17日,我国神舟十一号载人飞船顺利升空.航天领域涉及许多化学知识,请你完成下列各题.
(1)运载火箭使用的燃料之一为偏二甲肼(C2H8N2).偏二甲肼中碳、氢、氮元素的质量比为 .
(2)科学家利用铁酸镍(NiFe2O4)将航天员呼出的废气转化为航天员需要的气体,铁酸镍(NiFe2O4)中Ni显+2价,则Fe的化合价为 .
(3)宇航员舱外服实际上是个独立的狭小空间,废气处理系统保障着宇航员的生命.该系统让呼吸产生的废气进入一个装有活性炭的滤网除去有害气体,这一过程利用了活性炭的作用;同时用氢氧化锂(LiOH)作吸收剂除去二氧化碳,并生成碳酸锂和水,此反应的化学方程式为 .
(4)太阳能电池帆板用到了砷化镓(GaAs),镓元素在元素周期表中有如图所示信息.下列有关说法错误的是 . (填字母序号)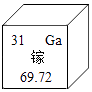
A.镓属于金属元素
B.镓的原子核内有31个质子
C.镓的相对原子质量为69.72
D.镓的原子核内有31个中子.
【答案】
(1)6:2:7
(2)+3
(3)吸附;2LiOH+CO2═Li2CO3+H2O
(4)D
【解析】解:(1)根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,可得偏二甲肼C2H8N2中碳、氢、氮元素的质量比为 (12×2):8:(14×2)=6:2:7;6:2:7. (2)Ni的化合价为+2价,氧元素显﹣2价,设铁元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+2)+x×2+(﹣2)×4=0,则x=+3价;+3.(3)活性炭具有吸附性,能吸附异味和色素等,该系统让呼吸产生的废气进入一个装有活性炭的滤网除去有害气体,这一过程利用了活性炭的吸附作用.用氢氧化锂(LiOH)作吸收剂除去二氧化碳,并生成碳酸锂和水,反应的化学方程式为:CO2+2LiOH═Li2CO3+H2O;吸附;2LiOH+CO2═Li2CO3+H2O;(4)A、镓元素带“钅”字旁,属于金属元素,故选项说法正确.B、根据元素周期表中的一格可知,左上角的数字为31,表示原子序数为31;根据原子序数=核电荷数=质子数=核外电子数,则该元素的原子的核外电子数为31,故选项说法正确.C、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为69.72,故选项说法正确.D、根据元素周期表中的一格可知,左上角的数字为31,表示原子序数为31;根据原子序数=核电荷数=质子数=核外电子数,则该元素的原子的核内质子数和核外电子数均为31,而不是中子数为31,故选项说法错误.
故选:D.
【考点精析】认真审题,首先需要了解书写化学方程式、文字表达式、电离方程式(注意:a、配平 b、条件 c、箭号),还要掌握碳单质的物理性质及用途(单质碳的物理性质各异,而各种单质碳的化学性质却完全相同;金刚石和石墨的物理性质有很大差异的原因是:碳原子的排列不同)的相关知识才是答题的关键.