题目内容
11.下列离子符号书写正确的是( )| A. | 铁离子Fe | B. | 镁离子 Mg | C. | 硫酸根离子SO42- | D. | 钾离子K1+ |
分析 离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略,据此进行分析判断.
解答 解:A、铁离子的离子符号为Fe3+,故选项离子符号书写错误.
B、镁离子的离子符号为Mg2+,故选项离子符号书写错误.
C、硫酸根离子的离子符号为SO42-,故选项离子符号书写正确.
D、钾离子的离子符号为K+,故选项离子符号书写错误.
故选:C.
点评 本题难度不大,掌握离子符号的表示方法的区别(元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略)是正确解答此类题的关键.

练习册系列答案
相关题目
2.在锰酸钾(化学式为K2MnO4)中,锰元素的化合价是( )
| A. | +7 | B. | +6 | C. | +5 | D. | +4 |
6.为了探究燃烧的条件,某兴趣小组话动中,同学们按图1装置对“可燃物燃烧的条件”进行探究.探究过程中,大家对磷燃烧生成的大量白烟是否危害人体健康提出疑问.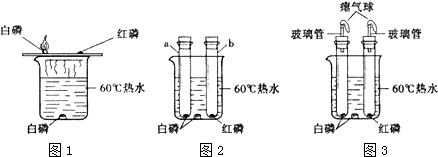
【查阅资料】白磷的着火点是40℃,红磷的着火点是240℃,…燃烧产物五氧化二磷是白色固体,会刺激人体呼吸道,可能与空气中水蒸气反应,生成有毒的偏磷酸(HPO3).
【变流与讨论】白烟对人体健康有害,该实验装置必须改进.
【改进与实验】同学们按改进后的图2装置进行实验.
请你帮助他们将下表补充完整.
【反思与评价】
(1)改进后的图2装置与图1装置比较,优点是防止白磷燃烧生成的五氧化二磷逸散到空气中,造成污染.
(2)王泽同学指出图2装置仍有不足之处,并设计了图3装置,其中气球的作用是:缓冲作用,防止胶塞冲出.
【拓展与迁移】
实验小结时,李颖同学说:“待a试管冷却恢复原温度后,如果将试管倒置水中,并在水中取下橡皮塞,将看到试管中液面升高.”这一说法得到大家的一致认同.
韩晶问:“如果不考虑橡皮塞占试管的容积,进入a试管内液体的体积会是多少呢?大家争论后,出现两种预测:甲:接近试管容积的$\frac{1}{5}$;乙:小于试管容积的$\frac{1}{5}$.
你赞同的预测是甲 (填“甲”或“乙”),理由是:空气中氧气的体积约占空气体积的$\frac{1}{5}$,且上述实验白磷足量、气密性良好,所以进入a试管内液体的体积能接近试管容积的$\frac{1}{5}$..

【查阅资料】白磷的着火点是40℃,红磷的着火点是240℃,…燃烧产物五氧化二磷是白色固体,会刺激人体呼吸道,可能与空气中水蒸气反应,生成有毒的偏磷酸(HPO3).
【变流与讨论】白烟对人体健康有害,该实验装置必须改进.
【改进与实验】同学们按改进后的图2装置进行实验.
请你帮助他们将下表补充完整.
| 现 象 | 解 释 |
| a试管中白磷燃烧,热水中白磷没有燃烧. b试管中红磷没有燃烧. | ①a试管中白磷燃烧的化学方程式是:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5; ②热水中白磷没有燃烧的原因是:达到着火点但没有和氧气接触; ③b试管中红磷没有燃烧的原因是:和氧气接触但没有达到着火点 |
(1)改进后的图2装置与图1装置比较,优点是防止白磷燃烧生成的五氧化二磷逸散到空气中,造成污染.
(2)王泽同学指出图2装置仍有不足之处,并设计了图3装置,其中气球的作用是:缓冲作用,防止胶塞冲出.
【拓展与迁移】
实验小结时,李颖同学说:“待a试管冷却恢复原温度后,如果将试管倒置水中,并在水中取下橡皮塞,将看到试管中液面升高.”这一说法得到大家的一致认同.
韩晶问:“如果不考虑橡皮塞占试管的容积,进入a试管内液体的体积会是多少呢?大家争论后,出现两种预测:甲:接近试管容积的$\frac{1}{5}$;乙:小于试管容积的$\frac{1}{5}$.
你赞同的预测是甲 (填“甲”或“乙”),理由是:空气中氧气的体积约占空气体积的$\frac{1}{5}$,且上述实验白磷足量、气密性良好,所以进入a试管内液体的体积能接近试管容积的$\frac{1}{5}$..
20.实验室里制取氢气和二氧化碳时,都可以选用的酸是( )
| A. | 稀HNO3 | B. | 稀HCl | C. | 稀H2SO4 | D. | 浓H2SO4 |
1.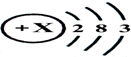 如表是元素周期表的一部分:
如表是元素周期表的一部分:
(1)12号元素的元素符号为Mg;Be元素的相对原子质量为9.012.
(2)相对原子质量为22.99的元素属金属(填“金属”或“非金属”);Ne的化学性质稳定(或不活泼);F元素最外层电子数为7.
(3)表中不同种元素最本质的区别是A(填字母).
A.质子数不同 B.相对原子质量不同 C.中子数不同
(4)元素周期表同一横行元素的排列规律是:从左至右金属元素→非金属元素→稀有气体元素(任写一点)
(5)如图为某元素的原子结构示意图,该元素位于周期表中第3周期第ⅢA族.
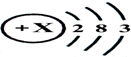 如表是元素周期表的一部分:
如表是元素周期表的一部分:| 族 周期 | IA | 0 | ||||||
| 一 | 1 H 1.008 | ⅡA | ⅢA | ⅣA | V A | ⅥA | ⅦA | 2 He 4.003 |
| 二 | 3 Li 6.941 | 4 Be 9.012 | 5 B 10.8l | 6 C 12.01 | 7 N 14.0l | 8 O 16.00 | 9 F 19.00 | 10 Ne 20.18 |
| 三 | 11 Na 22.99 | 12 Mg 24.31 | 13 Al 26.98 | 14 Si 28.09 | 15 P 30.97 | 16 S 32.06 | 17 Cl 35.45 | 18 Ar 39.95 |
(2)相对原子质量为22.99的元素属金属(填“金属”或“非金属”);Ne的化学性质稳定(或不活泼);F元素最外层电子数为7.
(3)表中不同种元素最本质的区别是A(填字母).
A.质子数不同 B.相对原子质量不同 C.中子数不同
(4)元素周期表同一横行元素的排列规律是:从左至右金属元素→非金属元素→稀有气体元素(任写一点)
(5)如图为某元素的原子结构示意图,该元素位于周期表中第3周期第ⅢA族.