题目内容
10.当CO与CO2质量比为2:3时,氧原子的个数比为多少?,若CO与CO2中氧原子个数比为3:4,则CO与CO2的质量比是多少?(提示:不同物质中同种原子个数比即为这种元素的质量比)分析 根据题意,不同物质中同种原子个数比即为这种元素的质量比,结合化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答 解:当CO与CO2质量比为2:3时,所含氧元素的质量比为(2×$\frac{16}{12+16}$×100%):(3×$\frac{16×2}{12+16×2}×$100%)=11:21,不同物质中同种原子个数比即为这种元素的质量比,则氧原子的个数比为11:21.
若CO与CO2中氧原子个数比为3:4,则一氧化碳与二氧化碳的分子数之比为3:2,则CO与CO2的质量比是(28×3):(44×2)=21:22.
答:氧原子的个数比为11:21;CO与CO2的质量比是21:22.
点评 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
20.在化学反应2A+B=2C中,设有6克A和B完全反应生成14克的C,若B的相对分子质量是32,则c 的相对分子质量为( )
| A. | 56 | B. | 28 | C. | 20 | D. | 44 |
1.下列关于物质的组成和构成的说法中正确的是( )
| A. | 物质都是由多种元素组成 | B. | 含有不同元素的物质一定是化合物 | ||
| C. | 任何物质都是由一种元素组成 | D. | 物质并不都是由分子构成的 |
18.下列属于纯净物的是( )
| A. | 清新的空气 | B. | 食盐水 | C. | 冰水混合物 | D. | 自来水 |
5.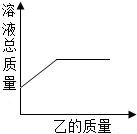 在一定质量的甲溶液中逐渐加入乙至过量,反应过程中溶液的总质量与加入乙的质量的关系如下图所示,表中物质能用图所示曲线表示的是( )
在一定质量的甲溶液中逐渐加入乙至过量,反应过程中溶液的总质量与加入乙的质量的关系如下图所示,表中物质能用图所示曲线表示的是( )
 在一定质量的甲溶液中逐渐加入乙至过量,反应过程中溶液的总质量与加入乙的质量的关系如下图所示,表中物质能用图所示曲线表示的是( )
在一定质量的甲溶液中逐渐加入乙至过量,反应过程中溶液的总质量与加入乙的质量的关系如下图所示,表中物质能用图所示曲线表示的是( ) | 序号 | 甲 | 乙 |
| ① | 稀盐酸 | 碳酸钠溶液 |
| ② | 稀盐酸 | 铁锈 |
| ③ | 稀硫酸 | 锌粒 |
| ④ | NaOH溶液 | 紫色石蕊试液 |
| A. | ①② | B. | ③④ | C. | ①③ | D. | ②③ |
11.图为甲、乙(均不含结晶水)的溶解度曲线,根据右图的溶解度曲线,判断下列叙述正确的是( ) 

| A. | t1℃甲、乙的饱和溶液升温到t2℃,变成不饱和溶液,溶质质量分数相等 | |
| B. | t2℃等质量的甲、乙溶液蒸发等质量的水,甲析出晶体多 | |
| C. | 甲中混有少量乙时,可以用蒸发的方法获得较纯净的乙 | |
| D. | t2℃等质量的甲、乙的饱和溶液降低温度到t1℃后溶液的质量相等 |

