题目内容
6. 水是人类生活中不可缺少的物质.
水是人类生活中不可缺少的物质.(1)净水时,通常用过滤的方法,除去水中难溶性杂质,常用活性炭做吸附剂除去水中的色素和异味.
(2)许莹同学设计了电解水简易装置,其中A、B电极由金属曲别针制成.通电后的现象如图所示.与A电极相连的试管中收集到的气体是氧气;电解水的文字表达式为:水$\stackrel{通电}{→}$氢气+氧气.电解水的符号表达式为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
(3)已知同温同压下,气体的体积比决定于气体的分子个数比.实验中能说明水的化学式为“H2O”的现象是氢气与氧气的体积比约为2:1.
(4)自来水中含有少量Ca(HCO3)2等可溶性化合物,烧水时Ca(HCO3)2发生分解反应,生成难溶性的碳酸钙、水和二氧化碳,这就是壶中出现水垢的原因之一.Ca(HCO3)2受热分解的文字表达式为碳酸氢钙$\stackrel{加热}{→}$碳酸钙+水+二氧化碳.符号表达式为Ca(HCO3)2 $\frac{\underline{\;\;△\;\;}}{\;}$CaCO3↓+H2O+CO2↑.
分析 (1)根据过滤可以除去不溶于水的物质;活性炭具有吸附性常用来去除水中的色素等解答;鉴
(2)根据电解水时与正极相连的试管中生成的气体较少是氧气;根据反应物和生成物以及质量守恒定律可以正确书写化学方程式.
(3)因为在化学变化中原子的种类及个数不会改变,所以反应后的氢氧原子数之比也是2:1,再结合氢分子和氧分子的构成情况与题目中给定的原理即可解决此题.
(4)根据反应物和生成物以及质量守恒定律可以正确书写化学方程式.
解答 解:(1)过滤可以除去不溶于水的物质;因为活性炭具有的吸附性,所以它常常用来去除水中的色素异味等杂质;
(2)电解水时A试管中生成的气体较少是氧气,B试管中生成的气体较多是氢气,解水的文字表达式为:水$\stackrel{通电}{→}$氢气+氧气;电解水的化学方程式为:2H2O $\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
(3)根据同温同压下体积比等于分子个数比,实验生成氢气和氧气的体积比为2:1,故氢分子和氧分子的分子个数比为2:1,同时由于氢分子和氧分子都是双原子分子,所以可知水分子中氢原子和氧原子的个数比为2:1,水分子的化学式是H2O.
(4)依据题干中的信息结合化学方程式的书写要求可知:Ca(HCO3)2受热分解生成碳酸钙、水和二氧化碳,受热分解的文字表达式为:碳酸氢钙$\stackrel{加热}{→}$碳酸钙+水+二氧化碳,反应的化学方程式为:Ca(HCO3)2 $\frac{\underline{\;\;△\;\;}}{\;}$CaCO3↓+H2O+CO2↑.
故答案为:
(1)过滤;活性炭;
(2)氧气,水$\stackrel{通电}{→}$氢气+氧气;2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;
(3)氢气与氧气的体积比约为2:1;
(4)碳酸氢钙$\stackrel{加热}{→}$碳酸钙+水+二氧化碳;Ca(HCO3)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCO3↓+CO2↑+H2O.
点评 本题主要考查净化水的方法和电解水等方面的知识,电解水时,要理解正极和负极上产生的气体分别是哪种物质,并且要掌握产生的气体的体积关系.

 新思维寒假作业系列答案
新思维寒假作业系列答案| A. |  过滤液体 | B. |  溶解固体 | C. |  蒸发溶液 | D. |  稀释浓硫酸 |
| A. | 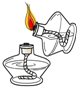 点燃酒精灯 | B. |  倾倒液体 | C. |  读液体体积 | D. |  过滤浑浊液 |