题目内容
15.利用下图装置在实验室模拟炼铁,并将得到的尾气中的一氧化碳和二氧化碳进行分离和收集.(提示:NaOH溶液可以吸收CO2气体.)实验步骤如下:(说明:M去掉,导管口加个气球,我不会加,让印刷厂给加上的)
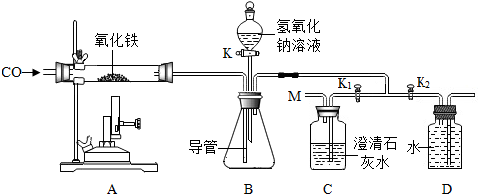
(1)检查装置气密性.
(2)取一定质量的氧化铁加入硬质玻璃管中,其它容器中各加入适量试剂(如图所示).
(3)关闭分液漏斗开关和K1,打开K2,通入CO气体一段时间,排除装置内的空气.
(4)打开分液漏斗开关K,将足量的氢氧化钠溶液放入锥形瓶中,使液面没过导管下端,关闭开关K.关闭K2,打开K1,继续通CO,点燃酒精喷灯,装置A的玻璃管中反应的化学方程是3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.当装置C中的现象是不变浑浊时,说明装置B中的反应是充分的,立即关闭K1,打开K2,装置D中收集到的气体是CO.
(5)一段时间后,停止加热,继续通CO气体至装置A的药品冷却.经称量氢氧化钠溶液增重2.64g,此时生成Fe的质量是2.2g(结果精确到0.1g).
分析 (4)根据反应原理来书写化学方程式以及氢氧化钙的性质来分析现象;
(5)氢氧化钠溶液增重的质量即反应中生成二氧化碳的质量,利用化学方程式进行计算.
解答 解:(4)在高温的条件下,一氧化碳与氧化铁反应生成铁和二氧化碳,反应的方程式是:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;二氧化碳进入B中,与氢氧化钠溶液反应,若C中澄清的石灰水不变浑浊则说明B中反应充分.
(5)氢氧化钠溶液增重2.64g,即一氧化碳还原氧化铁中生成的二氧化碳的质量,设生成铁的质量为x,则
3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
112 132
x 2.64g
$\frac{112}{132}=\frac{x}{2.64g}$ 解得:x≈2.2g
故答为:(4)3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,不变浑浊;(5)2.2;
点评 本题考查了根据化学方程式的计算,完成此题,可以依据题干提供的信息结合反应的化学方程式进行.

练习册系列答案
相关题目
10.实验室有两瓶标签破损的无色溶液,推知它们只能是碳酸钠溶液和硝酸钡溶液.某校兴趣小组的同学设计实验区分它们,请你参与实验,选择下列试剂进行区分,并回答有关问题.试剂:①pH试纸 ②KOH溶液 ③Ca(OH)2溶液 ④稀硫酸⑤Na2SO4溶液
| 所选试剂(填序号,每种方法只选择一种) | 实验现象及结论 | |
| 方法一 | ||
| 方法二 |
7.豆浆被称为“植物奶”,其中含有异黄酮(C15H10O2)具有防癌功能.那么下列关于异黄酮说法正确的是( )
| A. | 异黄酮中共含有27 个原子 | |
| B. | 一个异黄酮分子中含有一个氧分子 | |
| C. | 异黄酮中C、H、O三元素的质量比为15:10:2 | |
| D. | 异黄酮中碳元素质量分数最大 |
4.Mg3N2中N元素的化合价为( )
| A. | +2 | B. | +3 | C. | -2 | D. | -3 |


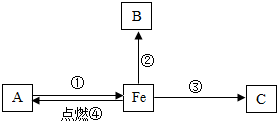 初中所学铁的部分化学性质如图所示(“→”表示物质间的转化关系,部分反应条件和物质已略去).
初中所学铁的部分化学性质如图所示(“→”表示物质间的转化关系,部分反应条件和物质已略去).