题目内容
8. “双吸剂”是常用的袋装食品的保鲜剂,可用来吸收氧气、二氧化碳、水蒸气等气体,某化学小组的同学在袋装食品中发现一包名为“504双吸剂”的保鲜剂,其标签如图所示.同学们对这包久置的“504双吸剂”的固体样品很好奇,设计实验进行探究.
“双吸剂”是常用的袋装食品的保鲜剂,可用来吸收氧气、二氧化碳、水蒸气等气体,某化学小组的同学在袋装食品中发现一包名为“504双吸剂”的保鲜剂,其标签如图所示.同学们对这包久置的“504双吸剂”的固体样品很好奇,设计实验进行探究.【提出问题】久置“双吸剂”的成分是什么?
[收集资料]:铁与氯化铁溶液在常温下生成氯化亚铁:Fe+2FeCl3=3FeCl2
【做出猜想】久置“双吸剂”中可能有Fe、Fe2O3、CaO、Ca(OH)2、CaCO3
【实验探究】如表是甲组同学涉及并记录的实验报告,请你补充完整.
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量固体研碎,和磁铁吸引 | 有少量黑色固体被吸引 | 固体中一定有含有铁粉 |
| ②取①中残留固体加入足量水,充分溶解并过滤,向滤液中通入CO2 | 发现滤液变浑浊 | 滤液中含有氢氧化钙 |
| ③向②的滤渣中加入足量稀盐酸 | 产生气泡,得到无色溶液 | 固体中一定含有CaCO3;一定不含有Fe2O3 |
(1)小刚认为固体中一定含有Ca(OH)2,小明认为不正确,其原因是氧化钙与水反应生成氢氧化钙;小明重新设计实验验证Ca(OH)2是否存在;取少量固体和氯化铵一起研磨,闻到有刺激性气味,因此确认固体中含有Ca(OH)2.
(2)③中反应的化学方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑.
[拓展交流]:铁粉作为食品保鲜剂的优点是能同时吸收氧气和水蒸气.
分析 【实验探究】二氧化碳能使澄清的石灰水变浑浊,是因为二氧化碳和石灰水中的氢氧化钙反应生成了碳酸钙沉淀和水,反应的化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O;
碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳;
氧化铁和稀盐酸反应生成氯化铁和水,氯化铁溶液是黄色的;
【反思提高】氧化钙和水反应生成氢氧化钙;
氢氧化钙和氯化铵反应生成氯化钙、水和氨气,氨气是一种有刺激性气味的气体;
[拓展交流]铁和水、氧气在一定条件下反应生成氧化铁.
解答 解:【实验探究】实验过程如下表所示:
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量固体研碎,和磁铁吸引 | 有少量黑色固体被吸引 | 固体中一定有含有铁粉 |
| ②取①中残留固体加入足量水,充分溶解并过滤,向滤液中通入CO2 | 发现滤液变浑浊 | 滤液中含有氢氧化钙 |
| ③向②的滤渣中加入足量稀盐酸 | 产生气泡,得到无色溶液 | 固体中一定含有CaCO3;一定不含有Fe2O3 |
小明重新设计实验验证Ca(OH)2是否存在:取少量固体和氯化铵一起研磨,闻到有刺激性气味,因此确认固体中含有Ca(OH)2.
故填:氧化钙与水反应生成氢氧化钙;氯化铵.
(2)③中反应的化学方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑.
故填:CaCO3+2HCl=CaCl2+H2O+CO2↑.
[拓展交流]铁粉作为食品保鲜剂的优点是能同时吸收氧气和水蒸气.
故填:能同时吸收氧气和水蒸气.
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

练习册系列答案
相关题目
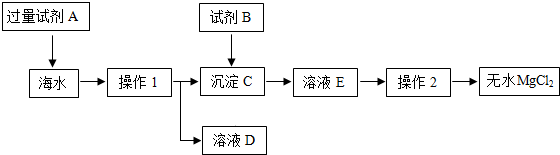
19.海水主要含有NaCl、MgCl2等物质,目前世界上60%的镁是从海水中提取的.小红同学模拟如图化工厂生产流程,以海水和贝壳(主要成分是碳酸钙)为原料来制取生产镁的原料----无水MgCl2.
(1)查阅资料.
氢氧化钠和氢氧化钙两种物质溶解度随温度变化表
(2)除杂过程
请回答:
①在30℃,试剂A最好选用:NaOH(填化学式).在海水中加入试剂A时发生反应的化学方程式是MgCl2+2NaOH=Mg(OH)2↓+2NaCl.
②若在实验室进行操作1,需要用到的玻璃仪器除漏斗、玻璃棒外,还有烧杯.
③试剂B与沉淀C发生反应的化学方程式是Mg(OH)2+2HCl=MgCl2+2H2O.
④MgCl2的相对分子质量是95,47.5g的MgCl2中含有12g的Mg.

(1)查阅资料.
氢氧化钠和氢氧化钙两种物质溶解度随温度变化表
| 温度(℃) 溶解度(g) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 |
| 氢氧化钠 | 42 | 51 | 109 | 119 | 129 | 145 | 174 | 299 | 314 | 329 |
| 氢氧化钙 | 0.18 | 0.17 | 0.16 | 0.15 | 0.14 | 0.13 | 0.12 | 0.105 | 0.095 | 0.08 |
请回答:
①在30℃,试剂A最好选用:NaOH(填化学式).在海水中加入试剂A时发生反应的化学方程式是MgCl2+2NaOH=Mg(OH)2↓+2NaCl.
②若在实验室进行操作1,需要用到的玻璃仪器除漏斗、玻璃棒外,还有烧杯.
③试剂B与沉淀C发生反应的化学方程式是Mg(OH)2+2HCl=MgCl2+2H2O.
④MgCl2的相对分子质量是95,47.5g的MgCl2中含有12g的Mg.
20.小光在做一氧化碳还原氧化铁的实验时,观察到玻璃管中的粉末由红棕色逐渐变为黑色,小光认为生成的黑色固体中可能含有金属铁,于是欲通过实验检验生成的黑色固体是否含有金属铁.请你帮他设计实验方案并填写下表.
上述表格中设计的实验方案中所发生反应的化学方程式为Fe+2HCl═FeCl2+H2↑.
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量黑色固体于试管中,向其中加稀盐酸. | 有气泡 产生. | 则黑色固体中含金属铁 |
17.下列实验现象的描述中,不正确的是( )
| A. | 硫在空气中燃烧,产生刺激性气味的气体 | |
| B. | 在点燃的蜡烛火焰上压一块白瓷板,白瓷板上有黑色烟点 | |
| C. | 氢气在空气中燃烧发出淡蓝色火焰 | |
| D. | 木炭在氧气中燃烧,发出白光,生成二氧化碳 |
3.做完氢氧化钠与稀硫酸中和反应的实验后,兴趣小组的同学对反应后溶液中的溶质成分产生了兴趣,请你与他们一起进行以下探究.
【提出问题】溶液中的溶质是什么物质?
【作出猜想】(1)甲同学认为溶液中的溶质只有Na2SO4一种物质.
(2)乙同学认为溶液中的溶质是Na2SO4和H2SO4两种物质.
(3)丙同学认为溶液中的溶质是Na2SO4和NaOH两种物质.
【查阅资料】(1)Na2SO4溶液显中性.
(2)Al与强碱NaOH溶液反应生成偏铝酸钠(NaAlO2)等物质.
【实验验证】
【总结反思】丁同学根据乙、丙两位同学的实验现象,首先肯定猜想(1)不成立.经过进一步分析,丁同学认为猜想(2)也不成立,他的理由是铝能和氢氧化钠反应生成偏铝酸钠和氢气.
兴趣小组的同学经过充分讨论,一致认为猜想(3)成立.
【知识拓展】(1)生活中能否用铝制品来盛放强碱性溶液?不能(填“能”或“不能”)
(2)乙同学的实验中铝片与氢氧化钠溶液发生了反应,请写出铝与该溶液发生反应的化学方程式2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
【提出问题】溶液中的溶质是什么物质?
【作出猜想】(1)甲同学认为溶液中的溶质只有Na2SO4一种物质.
(2)乙同学认为溶液中的溶质是Na2SO4和H2SO4两种物质.
(3)丙同学认为溶液中的溶质是Na2SO4和NaOH两种物质.
【查阅资料】(1)Na2SO4溶液显中性.
(2)Al与强碱NaOH溶液反应生成偏铝酸钠(NaAlO2)等物质.
【实验验证】
| 实验操作 | 实验现象 | 实验结论 | |
| 乙同学 实验 | 取中和反应后的溶液少许于试管中,将表面反复打磨后的铝片放入试管的溶液中 | 铝片逐渐溶解,并有大量气泡冒出,收集气体点燃,火焰呈淡蓝色 | 猜想(2)成立 |
| 丙同学 实验 | 取中和反应后的溶液少许于试管中,向试管中滴加几滴无色酚酞试液 | 溶液变红色 | 猜想(3)成立 |
兴趣小组的同学经过充分讨论,一致认为猜想(3)成立.
【知识拓展】(1)生活中能否用铝制品来盛放强碱性溶液?不能(填“能”或“不能”)
(2)乙同学的实验中铝片与氢氧化钠溶液发生了反应,请写出铝与该溶液发生反应的化学方程式2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
13. “双吸剂”是常用的袋装食品的保鲜剂,可用来吸收氧气、二氧化碳、水蒸气等气体.某化学小组的同学在袋装食品中发现一包名为“504双吸剂”的保鲜剂,其标签如图所示.同学们对这包久置的“504双吸剂”的固体样品很好奇,涉及实验进行探究.
“双吸剂”是常用的袋装食品的保鲜剂,可用来吸收氧气、二氧化碳、水蒸气等气体.某化学小组的同学在袋装食品中发现一包名为“504双吸剂”的保鲜剂,其标签如图所示.同学们对这包久置的“504双吸剂”的固体样品很好奇,涉及实验进行探究.
【提出问题】:久置固体的成分是什么?
【收集资料】:
1、查阅资料:铁与氯化铁溶液在常温下生成氯化亚铁:Fe+2FeCl3═3FeCl2
2、打开固体包装观察:部分粉末呈黑色、部分粉末呈白色、另有少数红棕色的块状固体.
【作出猜想】:久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2、CaCO3.
【实验探究】:如表是甲组同学涉及并记录的实验报告,请你补充完整.
【实验质疑】:乙组同学认为甲组同学在实验中得出“一定不含有Fe2O3”的结论是错误的,理由是氧化铁和盐酸反应生成氯化铁,铁和氯化铁反应生成氯化亚铁,溶液也是浅绿色;你认为甲组同学哪一步操作得出的结论也不合理操作二,理由是(用化学方程式表示)CaO+H2O=Ca(OH)2.
【继续探究】:为验证固体中是否含有Fe2O3,乙组同学用磁铁先分离出铁粉,向残留固体中加入足量稀盐酸,若溶液呈棕黄色,证明固体中含有Fe2O3.写出溶液呈棕黄色的化学反应方程式Fe2O3+6HCl=2FeCl3+3H2O.
 “双吸剂”是常用的袋装食品的保鲜剂,可用来吸收氧气、二氧化碳、水蒸气等气体.某化学小组的同学在袋装食品中发现一包名为“504双吸剂”的保鲜剂,其标签如图所示.同学们对这包久置的“504双吸剂”的固体样品很好奇,涉及实验进行探究.
“双吸剂”是常用的袋装食品的保鲜剂,可用来吸收氧气、二氧化碳、水蒸气等气体.某化学小组的同学在袋装食品中发现一包名为“504双吸剂”的保鲜剂,其标签如图所示.同学们对这包久置的“504双吸剂”的固体样品很好奇,涉及实验进行探究.【提出问题】:久置固体的成分是什么?
【收集资料】:
1、查阅资料:铁与氯化铁溶液在常温下生成氯化亚铁:Fe+2FeCl3═3FeCl2
2、打开固体包装观察:部分粉末呈黑色、部分粉末呈白色、另有少数红棕色的块状固体.
【作出猜想】:久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2、CaCO3.
【实验探究】:如表是甲组同学涉及并记录的实验报告,请你补充完整.
| 实验操作 | 实验现象 | 实验结论 |
| 一、取少量固体加入足量蒸馏水,搅拌溶解 | 固体部分溶解,并放出大量热 | 固体中一定含有CaO. |
| 二、过滤,取滤液滴加无色酚酞试液 | 溶液变红色 | 固体中一定含有氢氧化钙 |
| 三、取滤渣加入足量稀盐酸 | 固体逐渐消失,产生大量无色气体,得到浅绿色溶液 | 固体中一定含有Fe,一定不含有Fe2O3 |
| 四、将操作三中产生的气体通入到澄清石灰水中 | 澄清石灰水变浑浊 | 固体中一定含有CaCO3. |
【继续探究】:为验证固体中是否含有Fe2O3,乙组同学用磁铁先分离出铁粉,向残留固体中加入足量稀盐酸,若溶液呈棕黄色,证明固体中含有Fe2O3.写出溶液呈棕黄色的化学反应方程式Fe2O3+6HCl=2FeCl3+3H2O.