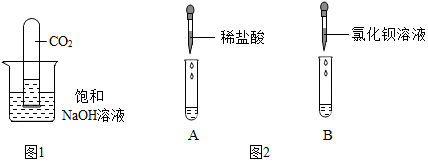
题目内容
2.下列各组离子在水中能大量共存,并形成无色透明溶液的是( )| A. | Mg2+、Ca2+、OH-、CO32- | B. | Na+、NH4+、Cl-、NO3- | ||
| C. | Fe3+、Ba2+、Cl-、SO42- | D. | H+、K+、MnO4-、SO42- |
分析 根据复分解反应的条件,离子间若能互相结合成沉淀、气体或水,则离子不能大量共存,据此进行分析判断即可.本题还要注意溶液呈无色,不能含有明显有颜色的铜离子、铁离子和亚铁离子等.
解答 解:A、Ca2+、CO32-两种离子能结合成碳酸钙沉淀,Mg2+、OH-两种离子能结合成氢氧化镁沉淀,不能大量共存,故选项错误.
B、四种离子间不能结合成沉淀、气体或水,能大量共存,且不存在有色离子,故选项正确.
C、Ba2+、SO42-两种离子能结合成硫酸钡沉淀,不能大量共存,且Fe3+的水溶液呈黄色,故选项错误.
D、四种离子间不能结合成沉淀、气体或水,能大量共存,但MnO4-的水溶液呈紫红色,故选项错误.
故选:B.
点评 本题考查了离子共存的问题,判断各离子在溶液中能否共存,主要看溶液中的各离子之间能否发生反应生成沉淀、气体、水;还要注意特定离子的颜色.

练习册系列答案
 春雨教育同步作文系列答案
春雨教育同步作文系列答案
相关题目
12.下列物品所使用的材料属于合金的是( )
| A. | 玻璃杯 | B. | 橡胶鞋 | C. | 不锈钢壶 | D. | 混凝土 |
10.在剧烈的高强度运动中,人体内的葡萄糖(C6H12O6)会进行无氧反应,产生乳酸(C3H6O3),下列说法正确的是( )
| A. | 葡萄糖是一种氧化物 | |
| B. | 葡萄糖不能为人体提供能量 | |
| C. | 一个葡萄糖分子中含有两个乳酸分子 | |
| D. | 葡萄糖与乳酸中碳元素的质量分数相同 |
17.“金、银、铜、铁、锡”俗称五金.这五种金属中,金属活动性最强的是( )
| A. | 铁 | B. | 金 | C. | 锡 | D. | 铜 |
7.已知NH4NO3和KH2PO4固体混合物中氮元素的质量分数为14%,则混合物中KH2PO4的质量分数为( )
| A. | 80% | B. | 60% | C. | 40% | D. | 20% |
14.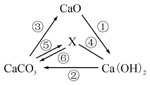 有关物质之间的部分转化关系如图所示.其中“-”表示物质之间能发生化学反应,“→”表示物质之间的转化关系.下列说法中正确的是( )
有关物质之间的部分转化关系如图所示.其中“-”表示物质之间能发生化学反应,“→”表示物质之间的转化关系.下列说法中正确的是( )
 有关物质之间的部分转化关系如图所示.其中“-”表示物质之间能发生化学反应,“→”表示物质之间的转化关系.下列说法中正确的是( )
有关物质之间的部分转化关系如图所示.其中“-”表示物质之间能发生化学反应,“→”表示物质之间的转化关系.下列说法中正确的是( )| A. | 物质X是一种常见的有机化合物 | |
| B. | 反应②是一定有盐参加反应 | |
| C. | 图中的所有反应均不属于置换反应 | |
| D. | 向Ca(OH)2溶液中加入CaO,所得溶液的溶质质量分数一定增大 |
11.下列对某一主题知识归纳都正确的一组是( )
| A、生活常识 | B、物质鉴别 |
| 洗涤剂洗油污:乳化作用 水银温度计原理:汞原子体积随温度升高而增大 | 黄金和黄铜:滴加稀盐酸 硬水和软水:观察是否澄清 |
| C、安全常识 | D、环境保护 |
| 油锅着火、电器着火:用水浇灭 火灾烟很大时:用湿毛巾捂住口鼻 | 减少水质污染:不使用含磷洗衣粉 减少温室效应:大力植树造林 |
| A. | A | B. | B | C. | C | D. | D |
12.下列排列顺序正确的是( )
| A. | 氮元素的化合价: | B. | 使用合金年代: | ||
| C. | 物质的溶解性: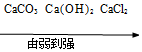 | D. | 铜元素的质量分数: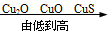 |