题目内容
实验室用100 g含杂质15%的大理石,最多可制得多少二氧化碳?
答案:
解析:
解析:
|
答:最多可制得二氧化碳37.4 g 解:设最多可制得二氧化碳的质量为x 由题意:纯净的CaCO3的质量为100 g×(1-15%)=85 g CaCO3 100 44 85 g x 100/85 g=44/x x=37.4 g 解析:由于化学方程式所表示的各物质之间的质量比是纯净物的质量比,不纯物质的质量不能直接用来根据化学方程式计算. (1)若已知物不纯,需先算出其中纯净物的质量:纯物质质量=不纯物质质量×纯物质质量分数=不纯物质量×(1-杂质质量分数),然后用纯物质质量根据化学方程式求出待求物质量. (2)若待求物不纯,需先根据方程式算出待求物中纯物质的质量,再求得待求物(不纯物)的质量. |

练习册系列答案
相关题目
某课外兴趣小组对实验室中的一瓶稀硫酸样品进行分析。他们分别用100 g稀硫酸与不同质量的锌粒(含杂质,杂质不与稀硫酸反应)反应,三次实验的数据如下表。
| 实验次数 | 1 | 2 | 3 |
| 加入 | 4 | 8 | 12 |
| 充分反应后剩余 物质的总质量(g) | 103.9 | 107.8 | 111.8 |
请回答下列问题:
(1)第 次实验,锌粒与稀硫酸恰好完全反应。
(2)计算该稀硫酸样品的溶质质量分数(写出计算过程)。
 工业上用铁矿石冶炼铁,他们在实验室用CO还原氧化铁,实验如图所示
工业上用铁矿石冶炼铁,他们在实验室用CO还原氧化铁,实验如图所示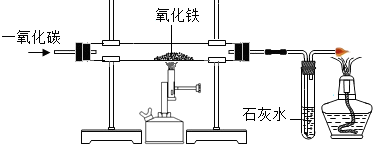 铁、铝、铜是日常生活中使用最广泛的金属.
铁、铝、铜是日常生活中使用最广泛的金属. 锌粒的质量(g)
锌粒的质量(g)