题目内容
12.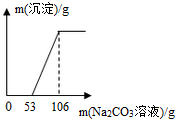 有氯化钙和盐酸的混合溶液100g,向混合溶液中加入碳酸钠溶液时生成沉淀的质量与所加入的碳酸钠的质量关系如图所示,若混合溶液中氯化钙的质量分数为5.55%,求原混合溶液中HCl的质量分数.
有氯化钙和盐酸的混合溶液100g,向混合溶液中加入碳酸钠溶液时生成沉淀的质量与所加入的碳酸钠的质量关系如图所示,若混合溶液中氯化钙的质量分数为5.55%,求原混合溶液中HCl的质量分数.
分析 根据碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,氯化钙和碳酸钠反应生成碳酸钙沉淀和氯化钠,依据题中氯化钙的质量和化学方程式计算碳酸钠的质量分数,然后依据化学方程式计算混合物中盐酸的质量分数.
解答 解:设碳酸钠的质量分数为x
Na2CO3+CaCl2=CaCO3+2NaCl
106 111
x×53g 100g×5.55%
$\frac{106}{53g×x}$=$\frac{111}{100g×5.55%}$
x=10%
设盐酸的质量质量分数为y
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 73
10%×53g x×100g
$\frac{106}{10%×53g}$=$\frac{73}{x×100g}$
x=3.65%.
故答案为:原混合溶液中HCl的质量分数为:3.65%.
点评 本题主要考查了化学方程式的计算,难度不大,注意解题的规范性和准确性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.向氯化铜溶液加入一定量的锌粉充分反应,下列情况中可能出现的是( )
| A. | 溶液中有 Zn2+、Cu2+,不溶物为Zn | B. | 溶液中有 Zn2+、Cu2+,不溶物为Cu | ||
| C. | 溶液只有 Zn2+,不溶物为 Zn、Cu | D. | 溶液只有 Zn2+,不溶物为 Cu |
17.具备基本的化学实验技能是进行化学探究活动的基础和保证,同时也反映了实验者的化学学科素养,以下实验操作正确的是( )
| A. | 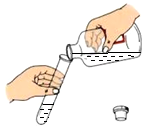 向试管中倾倒液体 | B. | 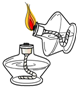 点燃酒精灯 | ||
| C. | 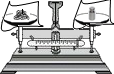 固体物质的称量 | D. |  加热固体物质 |
4.废旧手机的某些部件含有Mg、Al、Cu、Ag等金属,为了回收重金属,将旧手机部件浸入足量稀盐酸中充分反应后,过滤,所得固体中含有的金属是( )
| A. | Cu、Ag | B. | Mg、Ag | C. | Al、Cu | D. | Mg、Ag |
1.善于梳理化学知识,能使你头脑更聪明.以下有错误的一组( )
| A | 化学变化中的能量变化 | B | 化肥知识 |
| 蜡烛燃烧--放热反应 碳还原二氧化碳--吸热反应 | 钾肥作用--增强抗寒、抗旱能力 使用事项--不能与碱性物质共用 | ||
| C | 元素与人体健康 | D | 化学原理解释生活常识 |
| 缺锌--易引起食欲不振,发育不良 缺钙--易骨质疏松或得佝偻病 | 用氢氧化钠去油污--与油脂反应 用 汽油除去油污--溶解作用 |
| A. | A | B. | B | C. | C | D. | D |
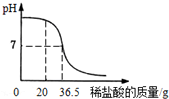 某化学兴趣小组在实验室配制一定溶质质量分数的稀盐酸,并用其测定某氢氧化钠溶液的溶质质量分数.
某化学兴趣小组在实验室配制一定溶质质量分数的稀盐酸,并用其测定某氢氧化钠溶液的溶质质量分数.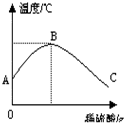 学习酸碱中和反应时,很多同学对其产生了探究兴趣.
学习酸碱中和反应时,很多同学对其产生了探究兴趣.