题目内容
15.有X、Y、Z三种金属,将它们分别投入稀盐酸中,Y无反应;如果把X、Z分别加入硫酸锌溶液中,X表面有锌析出,Z无变化.据此判断这三种金属的活动性由强到弱的顺序为( )| A. | X>Z>Y | B. | X>Y>Z | C. | Y>X>Z | D. | Z>X>Y |
分析 根据金属活动性顺序的意义进行分析,在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来.
解答 解:有X、Y、Z三种金属,将它们分别投入稀盐酸中,Y无反应,说明了X、Z的活动性大于Y;把X、Z分别加入硫酸锌溶液中,X表面有锌析出,Z无变化,说明金属的活动性X>Z,故三种金属的活动性由强到弱的顺序为X、Z、Y,所以A正确.
故选A.
点评 本题主要考查了金属活动性顺序表的应用,解答时可以依据金属活动性顺序表的应用及意义进行分析.

练习册系列答案
相关题目
6.实验室用100g溶质质量分数20%的双氧水与一定质量的二氧化锰混合制取氧气,为使反应慢点进行而又不影响生成氧气的质量,则下列操作不能达到目的是( )
| A. | 逐滴加入双氧水 | B. | 加水稀释 | ||
| C. | 减少双氧水的用量 | D. | 降低温度 |
10.欲除去不纯物质中的杂质(括号内为杂质),所用试剂不正确的是( )
| 选项 | 待提纯物质 | 选用试剂 |
| A | H2(H2O) | 浓硫酸 |
| B | NaCl(Na2CO3) | 盐酸 |
| C | CuSO4溶液(硫酸) | 氧化铜 |
| D | Fe(Cu) | 硫酸铜 |
| A. | A | B. | B | C. | C | D. | D |
20.下列反应属于中和反应的是( )
| A. | Fe+2HCl═FeCl2+H2↑ | B. | 2KMnO4$\frac{\underline{\;加热\;}}{\;}$K2MnO4+MnO2+O2↑ | ||
| C. | CaO+H2O═Ca(OH)2 | D. | Ca(OH)2+2HCl═CaCl2+2H2O |
7.下列常见物品中主要由天然有机材料制成的是( )
| A. | 不锈钢锅 | B. | 蚕丝丝巾 | C. | 塑料盆 | D. | 玻璃杯 |
4.下列物质的应用不正确的是( )
| A. |  不锈钢做硬币 | B. |  用亚硝酸钠腌渍鱼 | ||
| C. |  用硫酸填充蓄电池 | D. |  纯碱制洗涤剂 |
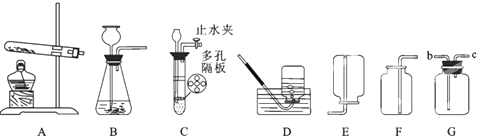


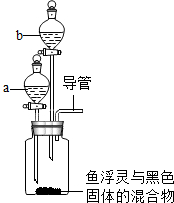 据调查,目前市场有一种产品叫“鱼浮灵”,放在鱼缸中可使水中的含氧量增加,某校科学小组的成员对“鱼浮灵”成分进行探究.
据调查,目前市场有一种产品叫“鱼浮灵”,放在鱼缸中可使水中的含氧量增加,某校科学小组的成员对“鱼浮灵”成分进行探究.