题目内容
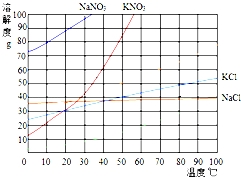
如图为几种固体的溶解度曲线,回答下列问题:
(1)NaCl的溶解度随温度变化的规律是 ;
(2) 20 ℃时KNO3和KCl的溶解度相等;
(3)50℃时,KCl溶液的最大浓度(列式即可)为 ;
(4)60℃时,10g NaCl和90g KNO3完全溶解于100g蒸馏水,冷却到20℃后, (“有”或“没有”)NaCl析出,有 g
KNO3结晶析出.
(5)现有一定温度下一定质量的NaCl溶液,将该溶液恒温蒸发10g水后析出了1g晶体,再恒温蒸发5g水后,又析出了2g克晶体,则保持温度不变,原溶液刚好达到饱和所需蒸发水的质量是 g.
【考点】固体溶解度曲线及其作用;晶体和结晶的概念与现象.
【专题】实验方法和过程的探究;溶液、浊液与溶解度.
【分析】根据物质的溶解度曲线可以判断随着温度的变化,物质的溶解度变化情况;
根据物质的溶解度曲线可以判断某一温度时物质的溶解度大小比较;
某温度下,饱和溶液的溶质质量分数最大,饱和溶液溶质质量分数= ×100%;
×100%;
根据物质的溶解度曲线、溶质质量、溶剂质量可以判断温度变化时是否析出晶体;
根据提供的数据可以进行相关方面的判断.
【解答】解:(1)NaC l的溶解度随温度变化的规律是.
l的溶解度随温度变化的规律是.
故填:随温度的升高而增大,但变化不大.
(2)20℃时KNO3和KCl的溶解度相等.
故填:20.
(3)50℃时,KCl的溶解度是40g,溶液的最大浓度为: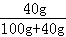 ×100%.
×100%.
故填: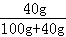 ×100%.
×100%.
(4)20℃时,氯化钠的溶解度大于35g,硝酸钾的溶解度是30g,60℃时,氯化钠的溶解度大于35g,硝酸钾的溶解度大于90g,10gNaCl和90gKNO3完全溶解于100g蒸馏水,冷却到20℃后,没有NaCl析出,有60gKNO3结晶析出.
故填:没有;60.
(5)将该溶液恒温蒸发10g水后析出了1g晶体,变成了饱和溶液,再恒温蒸发5g水后,又析出了2g克晶体,说明5g水溶解2g溶质恰好饱和,因此1g溶质溶解在2.5g水中恰好饱和,如果保持温度不变,原溶液刚好达到饱和所需蒸发水的质量是10g﹣2.5g=7.5g.
故填:7.5.
【点评】溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度不同;同一温度下,不同溶质的溶解度可能相同,也可能不同;温度对不同物质的溶解度影响不同.

 B.
B. C.
C. D.
D.