题目内容
13.二氧化碳和氢气可在一定条件下反应,生成一种重要的化工原料甲醇,化学方程式为:O2+3H2$\frac{\underline{\;钌-膦铬合物\;}}{加压}$CH3OH+H2O.下列有关该反应的说法正确的是( )| A. | 属于化学反应 | |
| B. | 钌-膦铬合物的质量在反应前后不变 | |
| C. | 反应前后原子的种类发生了变化 | |
| D. | 为CO2的利用创造了一种新途径 |
分析 A、根据反应的特征分析;
B、根据催化剂的特点分析;
C、利用二氧化碳合成新物质,实现的物质的综合利用;
D、根据反应物、生成物的种类可以判断反应类型.二氧化碳和氢气在一定条件下反应生成甲醇和水的过程中,钌-膦铬合物作催化剂,催化剂在反应前后的质量和化学性质不变化学反应遵循质量守恒定律,即反应前后元素的种类不变,原子的总个数不变
解答 解:A、该反应有新物质生成,属于化学反应,该选项说法正确;
B、钌-膦铬合物在反应中作催化剂,质量和化学性质不变.该选项说法正确;
C、原子在化学变中不可再分,所以,氢原子数在反应前后没有发生改变,该选项说法不正确;
D、利用二氧化碳合成甲醇,为二氧化碳的利用创造了一种新途径,该选项说法正确.
故选:ABD.
点评 二氧化碳在空气中的含量逐年增多,是造成温室效应的主要气体,实现二氧化碳的综合利用,既有利于保护环境,又有利于合成新物质,促进经济的发展.

练习册系列答案
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案
相关题目
3.某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动.以下是教学片段,请你参与学习并帮助填写空格(包括表中空格).
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的烧杯中.
【学生板演】该反应的化学方程式2NaOH+H2SO4═Na2SO4+2H2O.
Ⅰ.定性探究
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么呢?
猜 想】针对疑问大家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.你认为不合理的猜想是哪一种并说出理由猜想四,稀硫酸和氢氧化钠不能共存.
【继续实验】(1)丙组同学取烧杯中的少量溶液于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有氢氧化钠.
(2)为了验证其余猜想,各组同学取烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaC12溶液、Na2CO3溶液,分别进行如下三组探究实验.
【得出结论】通过探究,全班同学一致确定猜想二是正确的.
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定.同时指出上述三个实验探究中存在两处明显错误,请大家反思.同学们经过反思发现了这两处错误:(1)实验操作中明显的一处错误是把pH试纸浸入溶液中;
(2)实验方案探究中也有一个是不合理的,不合理的原因是滴加BaCl2溶液时,产生白色沉淀,不能说明溶液中有硫酸,因为硫酸钠能和氯化钡反应生成白色沉淀硫酸钡和氯化钠.
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的烧杯中.
【学生板演】该反应的化学方程式2NaOH+H2SO4═Na2SO4+2H2O.
Ⅰ.定性探究
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么呢?
猜 想】针对疑问大家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.你认为不合理的猜想是哪一种并说出理由猜想四,稀硫酸和氢氧化钠不能共存.
【继续实验】(1)丙组同学取烧杯中的少量溶液于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有氢氧化钠.
(2)为了验证其余猜想,各组同学取烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaC12溶液、Na2CO3溶液,分别进行如下三组探究实验.
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
| 实验操作 |  |  |  |
| 实验现象 | 试纸变色,比照比色卡,pH<7 | 产生气泡 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定.同时指出上述三个实验探究中存在两处明显错误,请大家反思.同学们经过反思发现了这两处错误:(1)实验操作中明显的一处错误是把pH试纸浸入溶液中;
(2)实验方案探究中也有一个是不合理的,不合理的原因是滴加BaCl2溶液时,产生白色沉淀,不能说明溶液中有硫酸,因为硫酸钠能和氯化钡反应生成白色沉淀硫酸钡和氯化钠.
4.家中烧开水的铝壶和盛放开水的暖瓶,使用时间长了易结水垢.原因是硬水中含有较多的可溶性的钙和镁的化合物,其中碳酸氢钙[Ca(HCO3)2]受热易分解,生成水和大量的气体,还生成一种难溶于水的化合物,它是水垢的主要成分.
[产生问题]碳酸氢钙受热分解除了生成水以外,另外两种生成物是什么?
[提出假设]
①小楠同学认为生成难溶于水的化合物可能是碳酸钙.
②小卓同学认为生成物中的气体可能是二氧化碳.
[实验与事实]依据猜想他们设计了如下实验方案:
[解释与结论]:水垢主要成分之一是碳酸钙.
请写出Ca(HCO3)2受热分解的化学方程式为:Ca(HCO3)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCO3↓+H2O+CO2↑.
[产生问题]碳酸氢钙受热分解除了生成水以外,另外两种生成物是什么?
[提出假设]
①小楠同学认为生成难溶于水的化合物可能是碳酸钙.
②小卓同学认为生成物中的气体可能是二氧化碳.
[实验与事实]依据猜想他们设计了如下实验方案:
| 实验步骤 | 实验现象 | |
| 验证猜想的①方案 | ①把适量难溶于水的化合物置于试管中,滴加稀盐酸 ②把生成的气体通入澄清石灰水中 | 有气泡生成 澄清石灰水变浑浊. |
| 验证猜想②的方案 | 取少量硬水于试管并加热,将生成气体通入 澄清石灰水中 | 澄清石灰水变浑浊 |
请写出Ca(HCO3)2受热分解的化学方程式为:Ca(HCO3)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCO3↓+H2O+CO2↑.
1.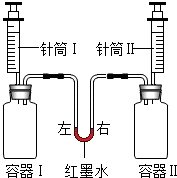 如图所示进行实验,同时将针筒内全部液体迅速注入容器中.实验内容如下表所示.
如图所示进行实验,同时将针筒内全部液体迅速注入容器中.实验内容如下表所示.
实验开始前红墨水左右两端液面保持相平,容器Ⅰ、Ⅱ体积相同,装置气密性良好.
(1)实验a中,容器Ⅰ内产生的现象是澄清石灰水变浑浊.
红墨水液面位置发生变化的原因是Ca(OH)2+CO2═CaCO3↓+H2O (用化学方程式表示).
(2)实验b中,针筒Ⅰ、Ⅱ内盐酸足量且溶质质量分数相同,产生气泡更剧烈的是容器Ⅱ (填“Ⅰ”或“Ⅱ”).红墨水液面位置变化情况是先是左高右低,最终红墨水左右两端液面保持相平.反应结束并恢复到原来的温度后,两边的红墨水保持相平.
 如图所示进行实验,同时将针筒内全部液体迅速注入容器中.实验内容如下表所示.
如图所示进行实验,同时将针筒内全部液体迅速注入容器中.实验内容如下表所示.实验开始前红墨水左右两端液面保持相平,容器Ⅰ、Ⅱ体积相同,装置气密性良好.
| 实验 编号 | 容器I | 针筒I | 容器Ⅱ | 针筒Ⅱ | 红墨水 液面位置 |
| a | 10mL 水 | NaCl | 10mL 水 | 保持 左高右低 | |
| b | 二氧化碳 (充满) | 10mL 澄清石灰水 | 二氧化碳 (充满) | 10mlL浓氢氧化钠溶液 | |
| c | 1g锌 | 15mL盐酸 | 1g镁 | 15mL盐酸 |
红墨水液面位置发生变化的原因是Ca(OH)2+CO2═CaCO3↓+H2O (用化学方程式表示).
(2)实验b中,针筒Ⅰ、Ⅱ内盐酸足量且溶质质量分数相同,产生气泡更剧烈的是容器Ⅱ (填“Ⅰ”或“Ⅱ”).红墨水液面位置变化情况是先是左高右低,最终红墨水左右两端液面保持相平.反应结束并恢复到原来的温度后,两边的红墨水保持相平.
8.对质量守恒定律的理解和应用,正确的是( )
| A. | 参加反应的氢气和氧气的体积.一定等于它们燃烧生成水的体积 | |
| B. | 反应前反应物的总质量等于反应后生成物的总质量 | |
| C. | 铜粉在空气中加热后固体质量增加,说明该变化不符合质量守恒定律 | |
| D. | 因为反应前后原子的种类和数目不变,所以反应前后物质总质量不变 |
5.下列物质分类中前者属于酸,后者属于碱的是( )
| A. | 硫酸钠,氢氧化钠 | B. | 盐酸,纯碱 | C. | 硫酸,烧碱 | D. | 碳酸钙,氧化钠 |
2.下列实验装置或实验操作中正确的是( )
| A. | 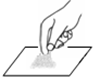 | B. | 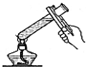 | C. |  | D. |  |
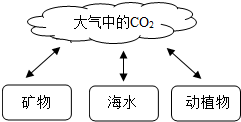 二氧化碳若合理利用,是一种重要的原料.
二氧化碳若合理利用,是一种重要的原料.