题目内容
10.CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O 的其中一个含义是:1体积的甲烷完全燃烧需要2体积的氧气,那么,在相同条件下,1体积的甲烷完全燃烧需要10体积的空气.分析 根据空气中氧气约占空气体积的$\frac{1}{5}$进行解答.
解答 解:空气中氧气约占空气体积的$\frac{1}{5}$,所以CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O 的其中一个含义是:1体积的甲烷完全燃烧需要2体积的氧气,那么,在相同条件下,1体积的甲烷完全燃烧需要空气的体积为2×5=10.
故答案为:10.
点评 掌握空气中氧气的含量是解题的关键,属于基础知识的考查.

练习册系列答案
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案
相关题目
1.目前常用的1元硬币(如图),其材质为( )


| A. | 纯铁 | B. | 钛合金 | C. | 钢芯镀铜 | D. | 钢芯镀镍 |
18.碳元素可形成多种单质和化合物,金刚石中碳元素的化合价是( )
| A. | 0 | B. | -4 | C. | +2 | D. | +4 |
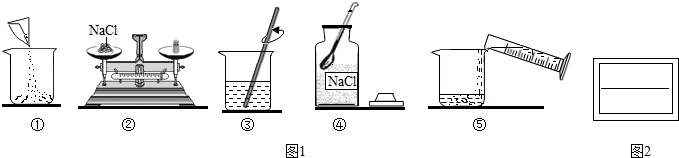
5.根据图表中实验现象,所得的结论错误的是( )
| 选项 | A | B | C | D |
| 实 验 |  |  |  |  |
| 实验 现象 | 向烧杯中加入氢氧化钠固体后,塑料片掉落 | 干冷的烧杯内壁有水珠出现 | 盐酸加入碳酸钠粉末中后,天平不再平衡 | 燃烧的蜡烛由低到高依次熄灭 |
| 实验 结论 | 氢氧化钠溶于水时会放热 | 气体X中含有氢元素 | 该反应不符合质量守恒定律 | 二氧化碳密度比空气大 |
| A. | A | B. | B | C. | C | D. | D |
2.下列关于金属和合金的叙述中错误的是( )
| A. | 合金的硬度一般比各成分金属大 | |
| B. | 生铁可以完全溶解在足量的稀盐酸中 | |
| C. | 金属与金属、金属与非金属都可能形成合金 | |
| D. | 长期使用铁锅烹调可以摄入铁元素从而预防缺铁性贫血 |
19.印染工业常用到硫化钠固体(Na2S),Na2S中硫元素的化合价是( )
| A. | -1 | B. | +1 | C. | -2 | D. | +2 |
20. 某天然矿泉水中元素及物质含量如表所示,请用相关化学用语回答下列问题.
某天然矿泉水中元素及物质含量如表所示,请用相关化学用语回答下列问题.
(1)表中的一种阴离子SO42-,或Cl-;
(2)标出偏硅酸中硅元素的化合价H2$\stackrel{+4}{Si}$O3;
(3)产自溶洞中的水中含有微量的二氧化碳,保持二氧化碳化学性质的最小粒子是CO2;
(4)在自来水厂净水方法中,说法正确的是③④
①通过沉淀、过滤、吸附除去水中难溶性杂质,就可得到纯净水
②常用的方法有:沉淀、吸附、过滤、蒸馏,其中净化程度最高的是蒸馏
③通过过滤的方法将不溶于水的固体杂质与水分离开
④用氯气给水杀菌是化学变化,用活性炭净化水是物理变化.
(5)自来水中含有少量Ca(HCO3)2等可溶性化合物,烧水时Ca(HCO3)2发生分解反应,生成难溶性的碳酸钙、水和二氧化碳,这就是壶中出现水垢的原因之一.请写出Ca(HCO3)2受热分解的化学方程式:Ca(HCO3)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCO3↓+H2O+CO2↑;
(6)有经验的鱼民在进行长途运输鲜鱼的过程中常常在水中加入少量的过氧化钙固体.已知过氧化氢的化学式可表示为H2O2,过氧化钾为K2O2,则过氧化钙的化学式为CaO2,若过氧化钾与水反应的方程式表示为2K2O2+2H2O=4KOH+O2↑,则过氧化钙与水的反应方程式为2CaO2+2H2O═2Ca(OH)2+O2↑,请说出使用过氧化钙可以使鱼长期存活的理由:与水反应生成氧气.
 某天然矿泉水中元素及物质含量如表所示,请用相关化学用语回答下列问题.
某天然矿泉水中元素及物质含量如表所示,请用相关化学用语回答下列问题.| 矿泉水中主要成分(mg/L) | |
| 偏硅酸(H2SiO3)30-50 硫酸根3-8 氯离子1-5 | 钙7-20 钠3-16 钾2-8 镁6-20 |
(2)标出偏硅酸中硅元素的化合价H2$\stackrel{+4}{Si}$O3;
(3)产自溶洞中的水中含有微量的二氧化碳,保持二氧化碳化学性质的最小粒子是CO2;
(4)在自来水厂净水方法中,说法正确的是③④
①通过沉淀、过滤、吸附除去水中难溶性杂质,就可得到纯净水
②常用的方法有:沉淀、吸附、过滤、蒸馏,其中净化程度最高的是蒸馏
③通过过滤的方法将不溶于水的固体杂质与水分离开
④用氯气给水杀菌是化学变化,用活性炭净化水是物理变化.
(5)自来水中含有少量Ca(HCO3)2等可溶性化合物,烧水时Ca(HCO3)2发生分解反应,生成难溶性的碳酸钙、水和二氧化碳,这就是壶中出现水垢的原因之一.请写出Ca(HCO3)2受热分解的化学方程式:Ca(HCO3)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCO3↓+H2O+CO2↑;
(6)有经验的鱼民在进行长途运输鲜鱼的过程中常常在水中加入少量的过氧化钙固体.已知过氧化氢的化学式可表示为H2O2,过氧化钾为K2O2,则过氧化钙的化学式为CaO2,若过氧化钾与水反应的方程式表示为2K2O2+2H2O=4KOH+O2↑,则过氧化钙与水的反应方程式为2CaO2+2H2O═2Ca(OH)2+O2↑,请说出使用过氧化钙可以使鱼长期存活的理由:与水反应生成氧气.