题目内容
5.根据图原子结构示意图填空: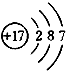
该元素的元素符号为:Cl.在化学中反应中它的原子易得到电子,变成阴(阴或阳)离子,其离子符号为Cl-.
分析 原子结构示意图中,圆圈内数字表示核内质子数,弧线表示电子层,弧线上的数字表示该层上的电子数,离圆圈最远的弧线表示最外层.若最外层电子数≥4,在化学反应中易得电子,若最外层电子数<4,在化学反应中易失去电子.
解答 解:由图中的原子结构示意图,该原子的核内质子数为17,为氯元素,其元素符号为Cl;其最外层电子数是7,在化学反应中易得到1个电子而形成带1个单位负电荷的阴离子,其离子符号为:Cl-.
故答案为:Cl;得到;阴;Cl-.
点评 本题难度不大,考查学生对原子结构示意图及其意义的理解,了解原子结构示意图的意义是正确解题的关键.

练习册系列答案
相关题目
3.下列化学现象的描述,正确的是( )
| A. | 铁丝在空气中剧烈燃烧,火星四射,生成黑色固体 | |
| B. | 硫在氧气中燃烧,发出蓝紫色火焰 | |
| C. | 木炭在氧气中燃烧比在空气中燃烧更旺,发出白光,并放出热量 | |
| D. | 红磷在氧气中燃烧产生白雾 |
13.某科学兴趣小组的同学,将实验室中某钢样品(假设钢样品中只含铁和碳),分成完全相同的质量为2.84g、4.26g、6.23g的三份,分别加入100g稀硫酸中进行实验(实验I、Ⅱ、Ⅲ),充分反应后,得到的实验数据如下表所示.下列分析中错误的是( )
| 实验I | 实验Ⅱ | 实验Ⅲ | |
| 样品质量(g) | 2.84 | 4.26 | 6.23 |
| 加入稀硫酸质量(g) | 100 | 100 | 100 |
| 产生氢气质量(g) | 0.10 | 0.15 | 0.20 |
| A. | 实验I中,铁已完全参加反应 | |
| B. | 实验Ⅱ,铁参加反应的质量为4.2g | |
| C. | 实验Ⅲ中,稀硫酸已完全参加反应实验 | |
| D. | 反应中所用稀硫酸的溶质质量分数为4.9% |
20.某探究小组的同学用H2SO4、Na2CO3、NaOH、BaCl2四种溶液进行“复分解反应发生条件”及应用的实验探究.
(1)将四种溶液两两混合,若用H2SO4与另三种溶液分别混合:
①实验中,能直接观察到说明H2SO4与Na2CO3溶液发生化学反应的证据是:有气体生成
②实验中的H2SO4与NaOH混合“无明显现象”,但实际上发生了化学反应,其反应的实质是H+和OH-结合生成H2O.同理,H2SO4与BaCl2发生了化学反应,其反应的实质是Ba2+和SO${\;}_{4}^{2-}$生成硫酸钡沉淀
由此同学们总结得出:复分解反应发生的条件是有沉淀或气体或水生成.
(2)若某复分解反应的生成物中有MgCl2,请写出可能的一组的反应物是盐酸与氢氧化镁
(3)若将原四种溶液混合反应后过滤,滤液经检验呈碱性且不含Ba2+、SO42-,取滤液少量,加入BaCl2溶液,无沉淀产生,再滴入几滴酚酞试液,溶液变红色,则滤液中存在的离子有OH-.
(1)将四种溶液两两混合,若用H2SO4与另三种溶液分别混合:
| Na2CO3 | NaOH | BaCl2 | |
| H2SO4 |
②实验中的H2SO4与NaOH混合“无明显现象”,但实际上发生了化学反应,其反应的实质是H+和OH-结合生成H2O.同理,H2SO4与BaCl2发生了化学反应,其反应的实质是Ba2+和SO${\;}_{4}^{2-}$生成硫酸钡沉淀
由此同学们总结得出:复分解反应发生的条件是有沉淀或气体或水生成.
(2)若某复分解反应的生成物中有MgCl2,请写出可能的一组的反应物是盐酸与氢氧化镁
(3)若将原四种溶液混合反应后过滤,滤液经检验呈碱性且不含Ba2+、SO42-,取滤液少量,加入BaCl2溶液,无沉淀产生,再滴入几滴酚酞试液,溶液变红色,则滤液中存在的离子有OH-.
17.人的机体活动和维持恒定体温需要能量.下列能为人体提供能量的物质是( )
| A. | 食盐 | B. | 维生素A | C. | 矿泉水 | D. | 花生油 |
14.绿色化学又称环境友好化学,它的主要特点之一是:提高原子的利用率,使原料中所有的原子全部转化到产品中,实现“零排放”.下列反应符合绿色化学这一特点的是( )
| A. | 工业冶铁 Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$ 2Fe+3CO2 | |
| B. | 用生石灰制熟石灰 CaO+H2O═Ca(OH)2 | |
| C. | 实验室制取二氧化碳 CaCO3+2HCl═CaCl2+H2O+CO2↑ | |
| D. | 实验室制取氢气 Zn+H2SO4═ZnSO4+H2↑ |