题目内容
3.判断在水溶液中一定能大量共存的离子组是( )| A. | Na+、H+、Cl-、CO32- | B. | H+、Ba2+、Cl-、SO42- | ||
| C. | Cu2+、Na+、NO3-、OH- | D. | H+、K+、Cl-、SO42- |
分析 根据在水中的离子不能结合生成水、气体、沉淀,则离子就一定能大量共存来分析解答.
解答 解:A、因H+、CO32-能结合生成水和二氧化碳气体,则不能大量共存,故错误;
B、因Ba2+、SO42-能结合生成硫酸钡沉淀,则不能大量共存,故错误;
C、因Cu2+、OH-能结合生成氢氧化铜沉淀,则不能大量共存,故错误;
D、因离子不能结合生成水、气体、沉淀,则离子一定能大量共存,故正确;
故选D.
点评 本题考查离子的共存,学生应学会利用物质的溶解性来判断离子是否结合生成沉淀,则熟悉常见物质的溶解性是解答本题的关键.

练习册系列答案
相关题目
10.下列关于饱和溶液的说法正确的是( )
| A. | 蒸发溶剂能析出溶质的溶液一定是饱和溶液 | |
| B. | 降温能析出溶质的溶液一定是饱和溶液 | |
| C. | 还能再溶解该溶质的溶液是饱和溶液 | |
| D. | 一定温度下,某物质的饱和溶液的溶质质量分数一定大于它的不饱和溶液的溶质质量分数 |
11.下列变化属于化学变化的是( )
| A. | 湿衣服晾干 | B. | 纸张燃烧 | C. | 切黄瓜 | D. | 海水晒盐 |
15.下列符号通常用来表示微观意义而不表示宏观意义的是( )
| A. | H | B. | H2 | C. | 2H | D. | H2O |
 如图是钙元素的相关信息.
如图是钙元素的相关信息.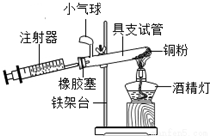 为测定空气中氧气的含量,小华同学打算设计如下方案:选用实际容积为50mL的具支试管作反应容器,将过量的铜粉放入试管,用橡皮塞塞紧具支试管,通过导管与实际容积为60mL且润滑性很好的针筒注射器组成如图的实验装置.请回答下列问题:
为测定空气中氧气的含量,小华同学打算设计如下方案:选用实际容积为50mL的具支试管作反应容器,将过量的铜粉放入试管,用橡皮塞塞紧具支试管,通过导管与实际容积为60mL且润滑性很好的针筒注射器组成如图的实验装置.请回答下列问题: