题目内容
以下是某研究小组探究影响反应速率部分因素的相关实验数据.| 实验序号 | 过氧化氢溶液浓度/% | 过氧化氢溶液体积/ml | 温度/C | 二氧化锰的用量/g | 收集氧气的体积/ml | 反应所用的时间/s |
| ① | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
| ② | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
| ③ | 30 | 5 | 35 | 2 | 49.21 | |
| ④ | 30 | 5 | 55 | 2 | 10.76 |
【答案】分析:(1)过氧化氢分解产生氧气和水,可以据此写出该反应的化学方程式;
(2)比较表格中的数据在其他条件都相同时,可以看出过氧化氢的浓度、温度等对化学反应速率的影响;
(3)物质在反应时接触面积越大,反应速率越快,反应物的浓度越大,在溶液中粒子间接触的机会更多,可以据此来解答该题;
(4)由于改变的只是溶液的浓度,但是溶质的质量没有改变,所以最终产生的氧气的质量不会改变;
(5)比较表格中的数据在其他条件都相同时,除了过氧化氢的浓度、温度之外,催化剂等对反应速率也有影响.
解答:解:(1)过氧化氢分解产生了氧气和水,所以可以写出该反应的化学方程式:2H2O2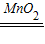 2H2O+O2↑;
2H2O+O2↑;
(2)从表中分析可知:①②中除了过氧化氢浓度不同之外,其他的各种量均相同,所以可以判断出是反应物的浓度影响了反应速率,并且是浓度越大,反应速率越快;③④则是温度不同其他条件相同,温度高的反应速率快;
(3)物质在反应时接触面积越大,反应速率越快,而反应物的浓度越大,在溶液中粒子间接触的机会更多,即粒子间碰撞的概率越大,所以反应速率也就越快;
(4)根据质量守恒定律可以知道,生成物的质量只与反应物的质量多少有关,而与反应物的浓度无关,所以本题中是向过氧化氢溶液中加入了水,而没有改变过氧化氢溶液中溶质的质量,所以产生氧气的质量不会改变;
(5)比较表中的数据可以知道,影响反应速率的因素除了温度和反应物的浓度之外,是否加入催化剂也能够影响反应的速率.
故答案为:
(1)2H2O2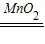 2H2O+O2↑;
2H2O+O2↑;
(2)反应物浓度;温度越高,化学反应速率越快;
(3)粒子间碰撞的概率越大,化学反应速率越快;
(4)不变;
(5)是否使用催化剂等.
点评:本题主要考查了能够影响化学反应的因素,解答这类题时要注意尽可能的把题中的能够影响化学反应的因素找出,然后再利用控制变量法来进行判断,最后得出答案.
(2)比较表格中的数据在其他条件都相同时,可以看出过氧化氢的浓度、温度等对化学反应速率的影响;
(3)物质在反应时接触面积越大,反应速率越快,反应物的浓度越大,在溶液中粒子间接触的机会更多,可以据此来解答该题;
(4)由于改变的只是溶液的浓度,但是溶质的质量没有改变,所以最终产生的氧气的质量不会改变;
(5)比较表格中的数据在其他条件都相同时,除了过氧化氢的浓度、温度之外,催化剂等对反应速率也有影响.
解答:解:(1)过氧化氢分解产生了氧气和水,所以可以写出该反应的化学方程式:2H2O2
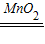 2H2O+O2↑;
2H2O+O2↑;(2)从表中分析可知:①②中除了过氧化氢浓度不同之外,其他的各种量均相同,所以可以判断出是反应物的浓度影响了反应速率,并且是浓度越大,反应速率越快;③④则是温度不同其他条件相同,温度高的反应速率快;
(3)物质在反应时接触面积越大,反应速率越快,而反应物的浓度越大,在溶液中粒子间接触的机会更多,即粒子间碰撞的概率越大,所以反应速率也就越快;
(4)根据质量守恒定律可以知道,生成物的质量只与反应物的质量多少有关,而与反应物的浓度无关,所以本题中是向过氧化氢溶液中加入了水,而没有改变过氧化氢溶液中溶质的质量,所以产生氧气的质量不会改变;
(5)比较表中的数据可以知道,影响反应速率的因素除了温度和反应物的浓度之外,是否加入催化剂也能够影响反应的速率.
故答案为:
(1)2H2O2
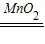 2H2O+O2↑;
2H2O+O2↑;(2)反应物浓度;温度越高,化学反应速率越快;
(3)粒子间碰撞的概率越大,化学反应速率越快;
(4)不变;
(5)是否使用催化剂等.
点评:本题主要考查了能够影响化学反应的因素,解答这类题时要注意尽可能的把题中的能够影响化学反应的因素找出,然后再利用控制变量法来进行判断,最后得出答案.

练习册系列答案
相关题目