题目内容
4.如图是某校课外学习小组设计的气体制取与性质验证的组合实验,请你参与有关实验并进行探究: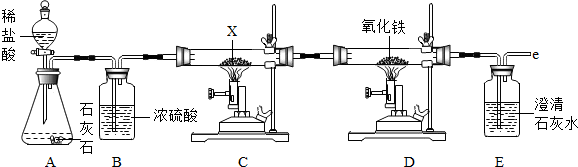
(1)请你帮他们写出C装置中发生反应的化学方程式:CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO.
(2)小红同学发现该装置中有一个明显的不足之处,即尾气没有处理直接排放到空气中.可采用图中V装置与上装置连接,从而改进完善上实验装置.
另一学习小组用酒精灯代替了上图D装置中的酒精喷灯,结果发现:反应后所得黑色粉末虽然能被磁铁吸附,但加入稀盐酸后却没有气泡出现,这引起了同学们的探究欲望.他们通过查阅资料并请教老师后得知:
(Ⅰ)该反应是分步进行的,且反应产物与反应温度有很大关系:
一氧化碳与氧化铁在加热的条件下发生如下反应:3Fe2O3+CO=2Fe3O4+CO2,Fe3O4+CO=3FeO+CO2,总反应式为Fe2O3+3CO=2Fe+3CO2.
(Ⅱ)FeO和Fe3O4都是黑色.
(Ⅲ)只有当温度高于700℃,FeO才可以大量被还原成单质铁.
同学们对(3)所得黑色粉末的成分提出如下猜想:
【提出猜想】甲同学猜想:Fe、Fe2O3和Fe3O4
乙同学猜想:2Fe3O4和FeO
丙同学猜想:Fe、Fe3O4和FeO
丁同学猜想:Fe、FeO
以上猜想中明显不合理的是:甲丙丁(填代号).
戊同学为了更准确的了解实验结果,他和本小组同学进行了一个定量实验,他们称取16.0g干燥的氧化铁(不含杂质),加热一段时间后隔绝空气冷却至室温,称量所得固体质量为14.6g,则该固体一定是混合物(选填“纯净物”或“混合物”)
【反思与评价】①生成的能被磁铁吸引的黑色固体不一定是“铁”;②欲验证反应产物是铁,还可用硫酸铜溶液,若看到有红色物质生成,就说明有单质铁生成,反应的化学方程式为Fe+CuSO4═FeSO4+Cu.
分析 (1)装置C是利用炭和二氧化碳来制取一氧化碳的,根据反应物、反应条件以及生成物来书写方程式;
(2)一氧化碳有毒,应该做一下尾气处理;
(3)【提出猜想】单质铁与盐酸反应会产生氢气;【反思与评价】根据金属的活动性分析.
解答 解:(1)由题意可知装置C中,炭粉与二氧化碳在高温的条件下反应生成一氧化碳,其化学方程式为:CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO;故填:CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO;
(2)一氧化碳有毒,会污染空气,所以应该将其燃烧,转化为二氧化碳或进行收集,又由于一氧化碳有毒,难溶于水,可用可用排水取气法收集.故答案为:尾气没有处理直接排放到空气中;V;
(3)【提出猜想】单质铁与盐酸反应会产生氢气;但实验中加入稀盐酸后却没有气泡出现,说明不会有单质铁;
根据Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
160 112
可知如果16.0g干燥的氧化铁全部转化为铁,剩余固体质量为11.2g
根据3Fe2O3+CO=2Fe3O4+CO2
160×3 232×2
可知如果16.0g干燥的氧化铁全部转化为铁,剩余固体质量为15.47g;
根据3Fe2O3+CO$\frac{\underline{\;高温\;}}{\;}$2Fe3O4+CO2,Fe3O4+CO$\frac{\underline{\;高温\;}}{\;}$3FeO+CO2,二者的总反应式
Fe2O3+CO$\frac{\underline{\;高温\;}}{\;}$2FeO+CO2
160 144
可知如果16.0g干燥的氧化铁全部转化为铁,剩余固体质量为14.4g;
所以.0g干燥的氧化铁(不含杂质),加热一段时间后隔绝空气冷却至室温,称量所得固体质量为14.6g,应为混合物;
【反思与评价】铁与硫酸铜反应生成硫酸亚铁和铜,会看到有红色物质生成,反应的方程式为:Fe+CuSO4═FeSO4+Cu.
故答案为:甲丙丁;混合物;硫酸铜;Fe+CuSO4═FeSO4+Cu.
点评 掌握一氧化碳与氧化铁反应的化学方程式;掌握铁的化学性质:与酸反应生成气体,与硫酸铜反应生成红色的铜;结合现象推测结论(反应本质).

 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案| A. | 焰心 | B. | 内焰 | C. | 外焰 | D. | 都一样 |
| A. |  测定溶液pH值 | B. |  稀释浓硫酸 | C. |  称取食盐 | D. |  固体药品的取用 |
| A. | 硫在空气中燃烧发出微弱的淡蓝色火焰 | |
| B. | 细铁丝在氧气中点燃,剧烈燃烧,火星四射,生成黑色固体 | |
| C. | 蜡烛在空气中燃烧产生大量白烟 | |
| D. | 红磷在氧气中燃烧,产生大量白烟 |
| A. |  观察液体体积 | B. |  给液体加热 | ||
| C. |  滴取少量液体 | D. |  细铁丝在氧气中燃烧 |
[提出猜想]人体呼出的气体中二氧化碳含量比空气中的二氧化碳含量多
[设计方案]用排水法收集一瓶呼出的气体,用另一集气瓶装一瓶空气,再分别检验其二氧化碳的含量
[进行实验]
| 实验步骤 | 实验现象 |
| 往两瓶气体中滴入等量的澄清石灰水,振荡 | 装有人体呼出气体的集气瓶中 变浑浊 装有空气的集气瓶中没有变化 |
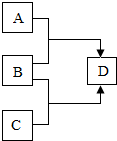 A、B、C、D为初中化学常见的物质,它们之间的转化关系如图所示(其中“→”表示转化关系).
A、B、C、D为初中化学常见的物质,它们之间的转化关系如图所示(其中“→”表示转化关系). 如图是有关氧气的知识结构图(部分反映条件省略.参加反应的氧气为足量).请回答下列问题:
如图是有关氧气的知识结构图(部分反映条件省略.参加反应的氧气为足量).请回答下列问题: