题目内容
20.利用能源、节约能源、保护环境是我们大家共同关注的社会问题.(1)海底埋藏着大银的“可燃冰”,可成为未来的新能源,其主要成分是甲烷水合物,甲烷的化学式CH4.
(2)煤燃烧时会排放出二氡化硫、二氧化氮等污染物,在一定条件下,二氧化硫与二氧化氮能发生反应:S02+N02=S03+X,其中X的化学式为NO,三氧化硫与氢氧化钠反应的化学方程式是SO3+2NaOH═Na2SO4+H2O
(3)生活中,人们常常利用煤燃烧反应产生的能量来做饭、取暖.下列有关说法正确的是C
A.化学反应过程中都会发生放热现象
B.在化学反应中只有燃烧反应才能放出热量
C.在当今社会,人类需要的大部分能量都是由化学反应产生的.
分析 (1)用元素符号和相应的数字可以表示物质的化学式.
(2)根据质量守恒定律可以判断物质的化学式,可以书写反应的化学方程式.
(3)化学反应中,有的放热,有的吸热;酸碱中和反应属于放热反应;人类需要的大部分能量是由化学反应产生的.
解答 解:(1)甲烷的化学式是:CH4.
故答案为:CH4.
(2)由质量守恒定律可知化学反应前后各原子的种类和个数不变,反应前硫、氧、氮原子的个数分别是1、4、1,而反应后硫、氧的原子个数分别是1、3,所以X中必含有一个氮原子和一个氧原子;所以X的化学式为NO.三氧化硫与氢氧化钠反应的化学方程式是SO3+2NaOH═Na2SO4+H2O.
故答案为:NO;SO3+2NaOH═Na2SO4+H2O.
(3)化学反应中,有的放热,有的吸热,酸碱中和反应属于放热反应,人类需要的大部分能量是由化学反应产生的.
故答案为:C.
点评 本题主要考查能源、化学方程式的书写等方面的知识,解答时要理解燃料燃烧生成物的性质,要根据质量守恒定律正确地书写化学方程式.

练习册系列答案
相关题目
2.根据下面的实验过程和提供的数据,可知样品中碳的质量分数为( )
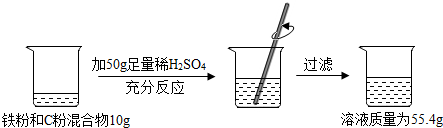

| A. | 44% | B. | 46% | C. | 54% | D. | 64% |
11.下列元素中,对人体有害的是( )
| A. | 钙(Ca) | B. | 铅(Pb) | C. | 锌(Zn) | D. | 铁(Fe) |
8.铁和四氧化三铁及其他含铁物质的性质、转换、用途是初中化学常见的知识内容.某兴趣小组同学在《培养中学生基本科学素养的化学实验教学研究》课题组老师的带领下开展了系列研究.
I:铁和四氧化三铁的转换:
i:铁在氧气里燃烧
【探究一】探究铁丝燃烧是否需要纯氧
【实验内容】取0.33mm的铁丝,分别在体积分数为90%、70%、65%、60%、55%的氧气中进行实验,实验现象:
【结论】就0.33mm铁丝而言,依据上表燃烧所需氧气的最低体积分数为60%,且氧气浓度越大,燃烧越剧烈.
【反思】所有铁丝的燃烧所需氧气最低浓度为上述结论不(填“是”或“不”)合理,理由是没有考虑铁丝的粗细.
ii:铁和四氧化三铁在转换时的应用:
在焊接两根铁轨时,为确保施工质量,工程技术人员常用到一种叫做“引火铁”的反应活性材料,“引火铁”(极细的铁粉)是一种准纳米材料,它在空气中可以自燃.某化学兴趣小组根据上述原理设计在实验室制备其过程如下:

(1)在高温条件下用普通铁粉和水蒸气反应,得到粉末状的四氧化三铁和氢气.
(2)将四氧化三铁粉末再在高温条件下经过与上述过程相反的反应生成“引火铁”粉末.请分别用以下两套装置,制取四氧化三铁和“引火铁”.(注:装置中必要的铁架台、铁夹、铁圈、石棉网、加热设备等在图1中均已略去)
填写下列空白:
(1)写出实验过程中第(1)、(2)两个步骤中的任一反应方程式:3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2,Fe3O4+4H2$\frac{\underline{\;高温\;}}{\;}$3Fe+4H2O;
(2)在实验装置中,烧瓶B的作用是产生水蒸气;
(3)实验时试管A中加入的固体是普通铁粉;
(4)在试管H中反应进行H2还原Fe3O4前,在I出口处必须先检验氢气的纯度.
II:在实验室中模拟炼铁化学原理的实验,对固体产物成分等进行探究
【设计实验】用一氧化碳还原纯净的氧化铁粉末,实验装置如图2.

【进行实验】该小组按上述实验设计,在一定温度下进行了实验,测得下列数据:
①反应前玻璃管和内盛氧化铁粉末的总质量66g(玻璃管的质量为60g)
②反应后玻璃管和内盛黑色固体的总质量65.8g(冷却到室温称量)
【得出结论】通过实验中获得的数据进行计算,得出黑色固体粉末为Fe3O4.
【反思与评价】一氧化碳还原氧化铁的实验中,可能会生成四氧化三铁、氧化亚铁等,那么要提高含铁量可采用的方法是延长通入CO的时间、提高反应温度、延长反应时间(答出一个即可).
I:铁和四氧化三铁的转换:
i:铁在氧气里燃烧
【探究一】探究铁丝燃烧是否需要纯氧
【实验内容】取0.33mm的铁丝,分别在体积分数为90%、70%、65%、60%、55%的氧气中进行实验,实验现象:
| O2% | 90% | 70% | 65% | 60% | 55% |
实验现象 | 燃烧剧烈,燃烧时间长,效果好 | 燃烧比90%弱,燃烧时间短,实验成功 | 燃烧比70%弱,燃烧时间比70%短,实验成功 | 燃烧比65%弱,燃烧时间更短,实验成功 | 难以燃烧,只是发红 |
【反思】所有铁丝的燃烧所需氧气最低浓度为上述结论不(填“是”或“不”)合理,理由是没有考虑铁丝的粗细.
ii:铁和四氧化三铁在转换时的应用:
在焊接两根铁轨时,为确保施工质量,工程技术人员常用到一种叫做“引火铁”的反应活性材料,“引火铁”(极细的铁粉)是一种准纳米材料,它在空气中可以自燃.某化学兴趣小组根据上述原理设计在实验室制备其过程如下:

(1)在高温条件下用普通铁粉和水蒸气反应,得到粉末状的四氧化三铁和氢气.
(2)将四氧化三铁粉末再在高温条件下经过与上述过程相反的反应生成“引火铁”粉末.请分别用以下两套装置,制取四氧化三铁和“引火铁”.(注:装置中必要的铁架台、铁夹、铁圈、石棉网、加热设备等在图1中均已略去)
填写下列空白:
(1)写出实验过程中第(1)、(2)两个步骤中的任一反应方程式:3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2,Fe3O4+4H2$\frac{\underline{\;高温\;}}{\;}$3Fe+4H2O;
(2)在实验装置中,烧瓶B的作用是产生水蒸气;
(3)实验时试管A中加入的固体是普通铁粉;
(4)在试管H中反应进行H2还原Fe3O4前,在I出口处必须先检验氢气的纯度.
II:在实验室中模拟炼铁化学原理的实验,对固体产物成分等进行探究
【设计实验】用一氧化碳还原纯净的氧化铁粉末,实验装置如图2.

【进行实验】该小组按上述实验设计,在一定温度下进行了实验,测得下列数据:
①反应前玻璃管和内盛氧化铁粉末的总质量66g(玻璃管的质量为60g)
②反应后玻璃管和内盛黑色固体的总质量65.8g(冷却到室温称量)
【得出结论】通过实验中获得的数据进行计算,得出黑色固体粉末为Fe3O4.
【反思与评价】一氧化碳还原氧化铁的实验中,可能会生成四氧化三铁、氧化亚铁等,那么要提高含铁量可采用的方法是延长通入CO的时间、提高反应温度、延长反应时间(答出一个即可).
15.下列物质名称、俗名、化学式、分类一致的是( )
| A. | 冰、干冰、H2O、氧化物 | B. | 银、水银、Hg、单质 | ||
| C. | 乙醇、酒精、C2H5OH、碱 | D. | 碳酸钠、苏打、Na2CO3、盐 |
5.以你目前掌握的化学知识,你认为下列说法不正确的是( )
| A. | “雪碧””可乐”等碳酸型饮料的pH小于7,晃动后打开瓶盖,其pH将增大 | |
| B. | PM2.5指数已经成为一个重要的测控空气污染程度的指数 | |
| C. | 为了不造成浪费,人们可以放心食用经过滤、加热、沉降、分离等一系列处理后的清亮的“地沟油” | |
| D. | 人误食重金属盐中毒后,为减轻毒性,最好服用蛋清 |
13.下列不属于人体必需的微量元素是( )
| A. | 钙 | B. | 铁 | C. | 锌 | D. | 氟 |