题目内容
3.回答下列有关对比实验的相关问题: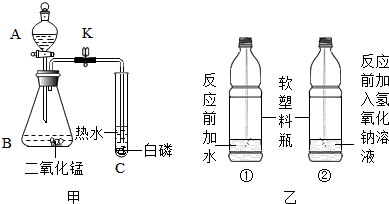
(1)实验甲,K在关闭时白磷不燃烧;打开K,并使A中液体进入B中,白磷燃烧,则B中发生反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,此实验得出的燃烧条件是与氧气接触.
(2)实验乙是利用体积相同并充满CO2的软塑料瓶、等体积的水(瓶①)和NaOH溶液(瓶②)进行实验对比的,证明CO2 与NaOH溶液中的溶质确实发生了反应的实验现象是瓶②比瓶①变瘪程度大.
分析 (1)通过甲图实验说明燃烧需要:与氧气接触;
(2)根据二氧化碳和NaOH溶液反应生成碳酸钠和水进行解答;
解答 解:(1)甲图实验:过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,要注意配平,其化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;通过图二实验说明可燃物燃烧需要与氧气接触;
(2)二氧化碳和NaOH溶液反应生成碳酸钠和水,二氧化碳被消耗,瓶内压强变小,软塑料瓶变瘪的程度变大;故填瓶②比瓶①变瘪程度大.
故答案为:
(1)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,与氧气接触;(2)瓶②比瓶①变瘪程度大.
点评 通过回答本题掌握了控制反应的发生和停止的实验装置的设计方法,学会了根据实验结论考虑实验目的,根据实验过程考虑所用仪器的方法.

练习册系列答案
 小学期末标准试卷系列答案
小学期末标准试卷系列答案
相关题目
13.今年4月22日是第46个世界地球日.今年地球日主题为:“珍惜地球资源、转变发展方式、提高资源利用效益”.保护地球是我们每个公民应尽的义务和责任,下列举措与这一主题相违背的是( )
| A. | 某些工业废水处理后再进行循环使用 | |
| B. | 积极开发使用风能和太阳能等新能源 | |
| C. | 为除瓜果蔬菜等农作物的虫害,推广使用剧毒农药 | |
| D. | 采用碳捕集和储存技术,逐步实现二氧化碳的零排放 |
14.2015年12月14日-16日,上海合作组织成员国政府首脑(总理)理亊会第十四次会议在郑州举行.14日晚欢迎宴会上的菜品或用料多与河南本地有关,如中原冷菜大拼盘、杞县紫薯泥、河南特色烩面等等.“紫薯泥”中富含下列哪种营养素( )
| A. | 蛋白质 | B. | 糖类 | C. | 油脂 | D. | 維生素 |
11.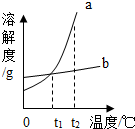 a、b两种物质的溶解度曲线如图所示.下列说法不正确的是( )
a、b两种物质的溶解度曲线如图所示.下列说法不正确的是( )
 a、b两种物质的溶解度曲线如图所示.下列说法不正确的是( )
a、b两种物质的溶解度曲线如图所示.下列说法不正确的是( )| A. | t1℃时,两种饱和溶液质量相等 | |
| B. | 将t2℃时a的饱和溶液降温至t1℃,溶液质量变小 | |
| C. | t2℃时,两种物质的饱和溶液中溶质质量分数a>b | |
| D. | 将t2℃时相同质量两种饱和溶液分别降温至t1℃,溶质质量a<b |
12.微粒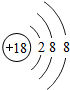 和
和 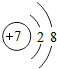 比较,相同的是( )
比较,相同的是( )
 和
和 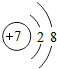 比较,相同的是( )
比较,相同的是( )| A. | 质子数 | B. | 电子层数 | C. | 最外层电子数 | D. | 所显电性 |