题目内容
3.写出稀硫酸与下列物质反应的化学方程式:①与铁粉反应:Fe+H2SO4═FeSO4+H2↑,
②与碳酸钠溶液反应:Na2CO3+H2SO4=Na2SO4+H2O+CO2↑,
③与氯化钡溶液反应:BaCl2+H2SO4═BaSO4↓+2HCl,
上述反应中,属于酸的共同性质的是①② (填编号).
分析 根据酸的化学性质(能与酸碱指示剂、活泼金属、金属氧化物、碱、碳酸盐等反应),由反应原理找出反应物、生成物、反应条件,由化学方程式的书写方法、步骤(写、配、注、等)进行书写,据此进行分析解答.
解答 解:①铁粉与稀硫酸反应生成硫酸亚铁溶液和氢气,反应的化学方程式:Fe+H2SO4═FeSO4+H2↑.
②碳酸钠溶液与稀硫酸反应生成硫酸钠、水和二氧化碳,反应的化学方程式:Na2CO3+H2SO4=Na2SO4+H2O+CO2↑.
③氯化钡溶液与稀硫酸反应生成硫酸钡沉淀和盐酸,反应的化学方程式:BaCl2+H2SO4═BaSO4↓+2HCl.
上述反应中,属于酸的共同性质的是①②,酸能与活泼金属、碳酸盐反应,与氯化钡溶液反应不是金属的共性,如稀盐酸不与氯化钡溶液反应.
故答案为:①Fe+H2SO4═FeSO4+H2↑;②Na2CO3+H2SO4=Na2SO4+H2O+CO2↑;③BaCl2+H2SO4═BaSO4↓+2HCl;①②.
点评 本题难度不大,掌握酸的化学性质(能与酸碱指示剂、活泼金属、金属氧化物、碱、碳酸盐等反应)并能灵活运用是正确解答本题的关键.

练习册系列答案
相关题目
11.下列说法中正确的是( )
| A. | 燃烧一定是化合反应,且一定有火焰 | |
| B. | 化合反应一定是由两种物质生成一种物质的化学反应 | |
| C. | 可燃物在氧气中燃烧一般均比在空气中燃烧更旺 | |
| D. | 氧气化学性质非常活泼,既可燃又能助燃 |
18.下列实验操作正确的是( )
| A. | 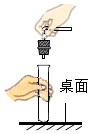 塞进橡皮塞 | B. | 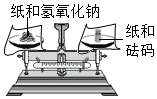 称取一定质量的氢氧化钠固体 | ||
| C. | 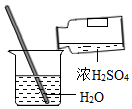 稀释浓硫酸 | D. | 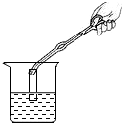 测定溶液的pH |
8.冬季我们北方某些地区室外“滴水成冰”.下列对“滴水成冰”过程中水分子变化的描述错误的是( )
| A. | 水分子能量降低 | B. | 水分子的运动速率减慢 | ||
| C. | 水分子之间间隔变小 | D. | 水分子的构成不变 |
15.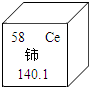 铈(Ce)是一种常见的稀土元素,如图是元素周期表中铈元素的信息示意图,对图中信息解释不正确的是( )
铈(Ce)是一种常见的稀土元素,如图是元素周期表中铈元素的信息示意图,对图中信息解释不正确的是( )
 铈(Ce)是一种常见的稀土元素,如图是元素周期表中铈元素的信息示意图,对图中信息解释不正确的是( )
铈(Ce)是一种常见的稀土元素,如图是元素周期表中铈元素的信息示意图,对图中信息解释不正确的是( )| A. | 原子序数是58 | B. | 铈元素是非金属元素 | ||
| C. | 质子数为58 | D. | 相对原子质量是140.1 |
 乳酸亚铁片可用于治疗缺铁性贫血.如图为乳酸亚铁片说明书上的部分内容.请仔细阅读后通过计算回答以下问题:
乳酸亚铁片可用于治疗缺铁性贫血.如图为乳酸亚铁片说明书上的部分内容.请仔细阅读后通过计算回答以下问题: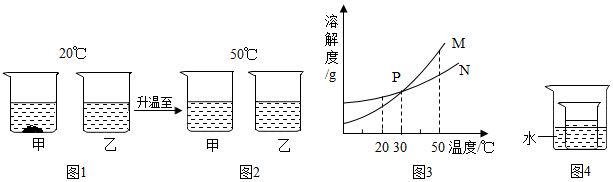
 如图是检查装置气密性的图示,请回答:
如图是检查装置气密性的图示,请回答: