题目内容
6.用“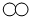 ”和“
”和“ ”分别代表两种不同的单质的分子A2和B2,它们在一定条件下能发生化学反应,其反应的微观示意图如图:
”分别代表两种不同的单质的分子A2和B2,它们在一定条件下能发生化学反应,其反应的微观示意图如图: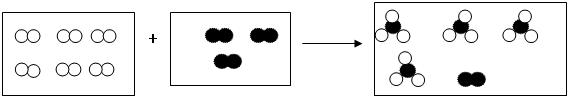
此反应类型为化合 反应,用化学方程式表示其反应为3A2+B2=2BA3.
分析 根据反应的微观示意图,分析反应物生成的构成特点写出化学式,再写出反应的化学方程式,根据反应的特点分析热反应的类型等.
解答 解:由反应的微观示意图可知,各物质反应的微粒数目关系是: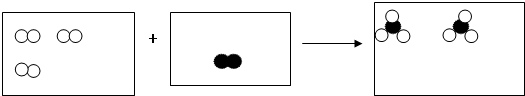 ,
,
由上图可知,此反应由两种物质生成了一种物质,类型为化合反应,用化学方程式表示其反应为:3A2+B2=2BA3.
故答为:化合 3A2+B2=2BA3
点评 本题通过微观粒子的反应模型图,考查了微观上对化学反应的认识,学会通过微观示意图把宏观物质和微观粒子联系起来、从微观的角度分析物质的变化是正确解答此类题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
14.在一定量的氢氧化钠稀溶液中逐渐滴加溶质质量分数为0.73%的稀盐酸,反应过程中不断搅拌并及时测量不同时刻溶液的温度与pH,记录数据如表:
(1)观察上表发现,当反应时间在125秒时,氢氧化钠与盐酸恰好中和.
(2)完成上述实验,能否用氢氧化钠固体代替请说明原因中和反应是放热反应,随盐酸量增加,中和反应放出热量增大,溶液温度上升;过量盐酸起冷却降温作用,反应停止热量散失,所以温度又会下降.
(3)结合上表中滴入稀盐酸体积与pH的变化数据,试计算氢氧化钠稀溶液中溶质的质量.(稀盐酸的密度取1.0克/毫升;化学方程式为:NaOH+HCl═NaCl+H2O)
| 反应时间(秒) | 0 | 25 | 50 | 75 | 100 | 125 | 150 | 175 | 200 |
| 滴入稀盐酸体积(毫升) | 0 | 4 | 8 | 12 | 16 | 20 | 24 | 28 | 32 |
| pH | 13.2 | 13.0 | 12.7 | 12.4 | 12.1 | 7.0 | 2.0 | 1.6 | 1.3 |
| 温度(℃) | 36.9 | 37.5 | 38.0 | 38.5 | 38.8 | 39.2 | 39.0 | 38.8 | 38.6 |
(2)完成上述实验,能否用氢氧化钠固体代替请说明原因中和反应是放热反应,随盐酸量增加,中和反应放出热量增大,溶液温度上升;过量盐酸起冷却降温作用,反应停止热量散失,所以温度又会下降.
(3)结合上表中滴入稀盐酸体积与pH的变化数据,试计算氢氧化钠稀溶液中溶质的质量.(稀盐酸的密度取1.0克/毫升;化学方程式为:NaOH+HCl═NaCl+H2O)
15.某同学测石膏(CuSO4•2H2O)中的结晶水含量,测得实验数据如下:
(1)石膏(CuSO4•2H2O)中结晶水含量的理论值是18.3%.
(2)表中实际测得的结晶水的含量是18.1%.
| 坩埚质量 | 坩埚与晶体总质量 | 加热后坩埚与固体总质量 | 测得晶体中结晶水的含量 |
| 11.7g | 22.7g | 20.7g |
(2)表中实际测得的结晶水的含量是18.1%.
16. 下列场所必须张贴如图所示的标志是( )
下列场所必须张贴如图所示的标志是( )
①煤矿;②液化气站;③加油站;④面粉厂;⑤纺织厂;⑥化工厂.
 下列场所必须张贴如图所示的标志是( )
下列场所必须张贴如图所示的标志是( )①煤矿;②液化气站;③加油站;④面粉厂;⑤纺织厂;⑥化工厂.
| A. | ①②③④ | B. | ②③④⑤⑥ | C. | ①②④⑤⑥ | D. | 全部 |
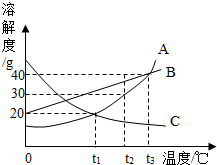 如图所示是A、B、C三种固体物质的溶解度曲线,
如图所示是A、B、C三种固体物质的溶解度曲线,