题目内容
2.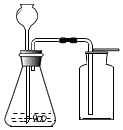 小亮同学设计如图装置来制取并收集气体,你认为他能制得的气体是( )
小亮同学设计如图装置来制取并收集气体,你认为他能制得的气体是( )| A. | 用KMnO4粉末制取O2 | B. | 用KClO3和MnO2制取O2 | ||
| C. | 用Zn和稀硫酸制取H2 | D. | 用石灰石和稀盐酸制取CO2 |
分析 此题考查了气体的制取装置和收集方法.从反应装置看,该装置选用的仪器是长颈漏斗和锥形瓶,所以适用于反应物是固体和液体,反应不需要加热的情况.从收集装置看,用的是向上排气法,所以收集的是气体比空气的密度大.
解答 解:A.用KMnO4粉末制取O2需要加热固体,图中发生装置不适合,故错误;
B.用氯酸钾和二氧化锰制取氧气的反应条件是加热,该装置没有酒精灯,故错误;
C.氢气的密度比空气小,排空气法收集氢气的方法是向下排空气法,图示是向上排空气法,故错误;
D.用石灰石和稀盐酸制取CO2,反应物是固体和液体反应,生成的二氧化碳密度比空气大,用向上排空气法收集,此项正确;
故选D.
点评 解此类题时,可以根据反应装置确定反应情况,也可以根据反应情况来确定反应的装置,因此要熟记常见气体的制取方法和收集方法.

练习册系列答案
 天天向上口算本系列答案
天天向上口算本系列答案
相关题目
10.2015年扬州市按空气质量标准评价达标天数比例为67.3%,共238天,空气质量轻度污染占25.1%,中度污染占5.6%,重度污染占2.0%.下列做法不利于改善扬州空气质量指数的是( )
| A. | 焚烧秸秆增加肥力 | B. | 城区严禁燃放烟花爆竹 | ||
| C. | 大力发展电力公交 | D. | 关闭燃煤小锅炉 |
17.生活中有太多的变化,下列“变”中涉及化学变化的是( )
| A. | 树根“变”根雕 | B. | 玉石“变”印章 | ||
| C. | 葡萄“变”美酒 | D. | 玩具机器人“变”形 |
6.从分子的角度分析,下列解释错误的是( )
| A. | 吹胀气球-气体分子间的间隔变大 | |
| B. | 浓氨水需要密封保存-分子在不断地运动 | |
| C. | 干冰升华-分子间间隔变大 | |
| D. | 过氧化氢分解成水和氧气-分子破裂、原子重新结合成新的分子 |
7.将一小块白色的金属钠放置在空气中会发生下列变化:
钠(Na)$\stackrel{O_{2}}{→}$钠的氧化物$\stackrel{H_{2}O}{→}$氢氧化钠溶液$\stackrel{CO_{2}}{→}$白色固体
【提出问题】常温下钠与氧气反应,产物有哪些?
【查阅资料】钠的氧化物,除氧化钠(Na2O)外还有过氧化钠(Na2O2),氧化钠与过氧化钠都能与水发生反应,方程式如下:Na2O+H2O═2NaOH;2Na2O2+2H2O═4NaOH+O2↑
【作出猜想】常温下钠与氧气反应的产物
猜想1:Na2O
猜想2:Na2O2
猜想3:Na2O和Na2O2
【实验探究一】:
【作出猜想】
猜想一:Na2CO3
猜想二:Na2CO3和NaOH
【实验反思】
(1)类比氧化铜与盐酸的反应,写出氧化钠与盐酸反应的化学方程式Na2O+2HCl=2NaCl+H2O;
(2)能与酸反应只生成盐和水的氧化物为碱性氧化物,请判断Na2O2不是碱性氧化物(填“是”或“不是”).
钠(Na)$\stackrel{O_{2}}{→}$钠的氧化物$\stackrel{H_{2}O}{→}$氢氧化钠溶液$\stackrel{CO_{2}}{→}$白色固体
【提出问题】常温下钠与氧气反应,产物有哪些?
【查阅资料】钠的氧化物,除氧化钠(Na2O)外还有过氧化钠(Na2O2),氧化钠与过氧化钠都能与水发生反应,方程式如下:Na2O+H2O═2NaOH;2Na2O2+2H2O═4NaOH+O2↑
【作出猜想】常温下钠与氧气反应的产物
猜想1:Na2O
猜想2:Na2O2
猜想3:Na2O和Na2O2
【实验探究一】:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量钠的氧化物加入足量蒸馏水 | 不产生气泡 | 猜想1正确 |
猜想一:Na2CO3
猜想二:Na2CO3和NaOH
| 实验操作 | 实验现象 | 实验结论 |
| 1.取少量白色固体加入足量 | 产生白色沉淀 | 白色固体成分为Na2CO3和NaOH |
| 2.过滤,取少量滤液加入 | 酚酞试液变红色 |
(1)类比氧化铜与盐酸的反应,写出氧化钠与盐酸反应的化学方程式Na2O+2HCl=2NaCl+H2O;
(2)能与酸反应只生成盐和水的氧化物为碱性氧化物,请判断Na2O2不是碱性氧化物(填“是”或“不是”).
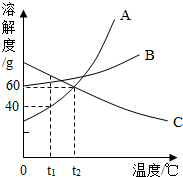 如图是A、B、C三种物质的溶解度曲线,回答下列问题:
如图是A、B、C三种物质的溶解度曲线,回答下列问题: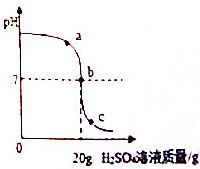 化学小组探究酸碱中和反应时,利用溶质质量分数为4.9%的稀硫酸来测定10gNaOH溶液样品的溶质质量分数,用数字化传感器测得溶液中pH的变化如图所示.
化学小组探究酸碱中和反应时,利用溶质质量分数为4.9%的稀硫酸来测定10gNaOH溶液样品的溶质质量分数,用数字化传感器测得溶液中pH的变化如图所示.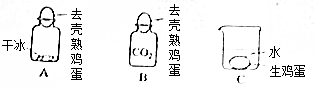 在一次科学实践活动课上,同学们做了“会动的鸡蛋”系列趣味实验.
在一次科学实践活动课上,同学们做了“会动的鸡蛋”系列趣味实验.