题目内容
16.ClO2是新一代自来水消毒剂,如图为制取ClO2反应的微观示意图.( )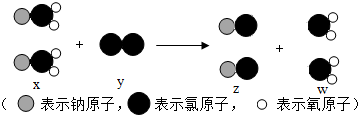
| A. | x是化合物,y单质 | |
| B. | z、w都是氧化物 | |
| C. | 该反应属于置换反应 | |
| D. | 该反应的化学方程式为:2NaClO2+Cl2═2NaCl+ClO2 |
分析 根据物质的微观构成,分析反应物、生成物,写出反应的化学方程式,根据反应的方程式进行有关的分析和判断.
解答 解:由制取ClO2反应的微观示意图中物质的微观构成可知,反应物是NaClO2和Cl2,生成物是NaCl和ClO2,反应的方程式是2NaClO2+Cl2═2NaCl+2ClO2,由此可知:
A、由以上分析可知X是NaClO2,由三种元素组成,属于化合物,Y是Cl2,属于单质,正确;
B、Z是氯化钠,不含有氧元素,不是氧化物,错误;
C、由上述分析可知,生成物是两种化合物,不属于置换反应,错误.
D、反应的化学方程式未配平,错误.
故选A.
点评 根据构成物质的分子的微观模型图,可判断分子的构成,由分子的构成可确定物质的组成及物质的化学式.再写出反应的方程式,由方程式即可进行有关的分析和判断.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.小亮在实验室发现一瓶盛有无色溶液的试剂瓶,其标签破损,从残余部分只能看出溶质的质量分数为10%,具体是什么物质无法辨认.老师告诉他,这瓶溶液可能是氢氧化纳、氯化钠、氢氧化钙或是碳酸钠中的一种.
(1)小亮查阅氢氧化钙常温下的溶解度为0.18g后,认为该溶液不可能是氢氧化钙,理由是Ca(OH)2微溶于水,常温下不可能得到10%的氢氧化钙溶液.
(2)小亮取少量样品于试管中,滴加无色酚酞 试液,试液变红色,该溶液不可能是NaCl(填写化学式),理由是NaCl溶液呈中性,不能使无色酚酞试液变红色.
(3)为了确定该溶液的成分,小亮同学继续进行下列实验,请一起参与,并填写下列实验报告.
【设计实验方案】方案甲:选择氯化钙溶液来确定该溶液的成份;方案乙:选择稀盐酸来确定该溶液的成份.
【进行实验】你愿意选择方案乙(选填“甲”或“乙”)进行实验.
(4)玉鹏同学认为还可以用一种不同于甲、乙类别的物质来确定,请你帮他完成,该物质可以为石灰水.
(1)小亮查阅氢氧化钙常温下的溶解度为0.18g后,认为该溶液不可能是氢氧化钙,理由是Ca(OH)2微溶于水,常温下不可能得到10%的氢氧化钙溶液.
(2)小亮取少量样品于试管中,滴加无色酚酞 试液,试液变红色,该溶液不可能是NaCl(填写化学式),理由是NaCl溶液呈中性,不能使无色酚酞试液变红色.
(3)为了确定该溶液的成分,小亮同学继续进行下列实验,请一起参与,并填写下列实验报告.
【设计实验方案】方案甲:选择氯化钙溶液来确定该溶液的成份;方案乙:选择稀盐酸来确定该溶液的成份.
【进行实验】你愿意选择方案乙(选填“甲”或“乙”)进行实验.
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量溶液于试管中,滴加氯化钙溶液(或稀盐酸). | 产生白色沉淀(或有气泡冒出) | 该溶液是碳酸钠溶液. 有关反应的化学方程式为: CaCl2+Na2CO3=CaCO3↓+2NaCl(或Na2CO3+2HCl=2NaCl+H2O+CO2↑). |
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量溶液于试管中,滴加该物质 | 产生白色沉淀 | 该溶液是碳酸钠溶液.有关反应的化学方程式为:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH |
1.下列实验现象描述不正确的是( )
| A. | 红磷在空气中燃烧产生大量白烟 | |
| B. | 镁在空气中燃烧,发出耀眼的白光,生成白色固体 | |
| C. | 铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体 | |
| D. | 硫在氧气中燃烧产生淡蓝色火焰,生成有刺激性气味的气体 |
5.工业冶炼金属铝的原理是2Al2O3=4Al+3O2↑,该反应属于( )
| A. | 置换反应 | B. | 化合反应 | C. | 分解反应 | D. | 复分解反应 |
6.2.2g某有机物在氧气中完全燃烧,生成6.6g二氧化碳和3.6g水(无其它生成物).下列对该物质组成的推断正确的是( )
| A. | 只含碳、氢元素 | B. | 含有碳、氢、氧三种元素 | ||
| C. | 含有碳、氢元素,可能含有氧元素 | D. | 碳、氢原子个数比为3:4 |
 ”表示氧原子,“
”表示氧原子,“ ”表示氢原子.请回答下列问题.
”表示氢原子.请回答下列问题.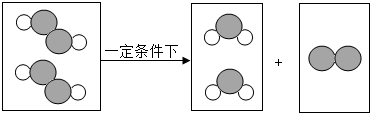

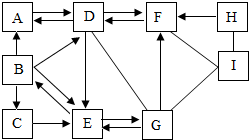 A-I是初中化学常见的物质,且都含有一种相同的元素,A、B、C、D、E是氧化物,白色固体F不溶于水,是最重要的建筑材料,它们之间的转化关系如图所示(“-”表示相邻的两物质可以发生反应,“→”表示箭头前面的物质可以转化为箭头后面的物质,部分反应的反应物、生成物和反应条件没有标出).
A-I是初中化学常见的物质,且都含有一种相同的元素,A、B、C、D、E是氧化物,白色固体F不溶于水,是最重要的建筑材料,它们之间的转化关系如图所示(“-”表示相邻的两物质可以发生反应,“→”表示箭头前面的物质可以转化为箭头后面的物质,部分反应的反应物、生成物和反应条件没有标出).