题目内容
11.请设计两种实验方案探究Mg、Fe、Cu三种金属的活动性顺序.(写出操作步骤、现象和结论)分析 在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来.设计实验证明金属的活动性顺序,可以使用活动性居中的金属为单质、强和弱的金属为盐溶液的方法,或是活动性居中的金属为盐溶液,强和弱的金属为单质的方法,也可以使用加酸观察是否产生气体的方法.
解答 解:方案一:在金属活动性顺序中,Mg>Fe>Cu,使用活动性强的金属镁和活动性弱的金属铜和用活动性中间金属铁的盐溶液进行试验,实验方案是:把镁和铜放入硫酸亚铁溶液中,镁表面有黑色物质析出,铜与硫酸亚铁不反应,证明镁的活动性比铁强,铁的活动性比铜强;
方案二:在金属活动性顺序中,Mg>Fe>Cu,使用活动性居中的金属铁单质,则需使用镁的盐溶液和铜盐溶液,实验方案是:将铁分别放入硫酸镁溶液和硫酸铜溶液中.铁不能与硫酸镁铁反应,铁在硫酸铜溶液中铁的表面有红色物质析出.证明镁的活动性比铁强,铁的活动性比铜银强;
故答为:方案一:把镁和铜放入硫酸亚铁溶液中,镁表面有黑色物质析出,铜与硫酸亚铁不反应,证明镁的活动性比铁强,铁的活动性比铜强;
方案二:将铁分别放入硫酸镁溶液和硫酸铜溶液中.铁不能与硫酸镁铁反应,铁在硫酸铜溶液中铁的表面有红色物质析出.证明镁的活动性比铁强,铁的活动性比铜银强.
点评 本类题属于明知故问型的题目,即在解答时根据已知的知识先判断金属活动性顺序然后再进行解答,所以要熟知金属活动性顺序的应用,以得到正确的解答.

练习册系列答案
相关题目
1.超氧化钠(NaO2)可用在呼吸面具中作为氧气的来源.
【资料】NaO2分别与CO2、H2O反应,都生成O2
【实验】验证在NaO2中通入CO2,反应产生O2
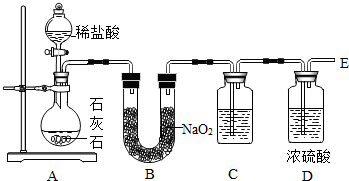
(1)上图装置不能(填“能”或“不能”)验证NaO2和CO2反应产生O2.
(2)要检验缓缓通入的CO2是否过量,C中盛放的试剂是澄清石灰水.
(3)证明生成O2的实验操作是:在E端放一个带火星的木条,木条复燃.
【问题】按图示装置实验,缓缓通入过量CO2后,U型管内剩余固体可能是什么?
【猜想】①可能是NaOH ②可能是Na2CO3 ③可能是NaOH和Na2CO3
(4)按要求完成表中相关内容:
①b中不能用Ba(OH)2溶液替代BaCl2溶液是因为Ba(OH)2与Na2CO3反应生成NaOH,影响对NaOH的检验.
②实验步骤b中所发生化学反应的方程式为BaCl2+Na2CO3=BaCO3↓+2NaCl.
【资料】NaO2分别与CO2、H2O反应,都生成O2
【实验】验证在NaO2中通入CO2,反应产生O2

(1)上图装置不能(填“能”或“不能”)验证NaO2和CO2反应产生O2.
(2)要检验缓缓通入的CO2是否过量,C中盛放的试剂是澄清石灰水.
(3)证明生成O2的实验操作是:在E端放一个带火星的木条,木条复燃.
【问题】按图示装置实验,缓缓通入过量CO2后,U型管内剩余固体可能是什么?
【猜想】①可能是NaOH ②可能是Na2CO3 ③可能是NaOH和Na2CO3
(4)按要求完成表中相关内容:
| 实验步骤 | 实验现象 | 实验结论 |
| a.取反应后装置B中全部固体,加水足量溶解 | (不填写) | 猜想③ 成立 |
| b.在上述溶液中加入足量BaCl2溶液 | 产生白色沉淀 | |
| c.在滤液中滴加少量酚酞试液 | 酚酞试液变红色 |
②实验步骤b中所发生化学反应的方程式为BaCl2+Na2CO3=BaCO3↓+2NaCl.
2.下列过程中,不属于化学变化的是( )
| A. |  改良酸性土壤 | B. |  用干冰进行人工降雨 | ||
| C. |  光合作用 | D. |  塑料降解 |
19.安多夫是一种嫩肉粉,成分是碳酸氢钠和氯化钠,小明发现将拌了安多夫粉的肉类放到锅中加入食醋等调料烧煮时会产生大量的气体,他对此颇感兴趣,决定对其进行探究.

【查阅资料】
(1)碳酸氢钠是白色细小晶体,加热到50℃以上开始逐渐分解生成碳酸钠、二氧化碳和水,440℃时完全分解.
(2)白色无水硫酸铜遇到水会变成蓝色.
【实验探究一】对烧煮时产生大量气体的探究
(1)小明对气体的成分进行了猜测:气体中除了醋酸气体之外,还可能含有水蒸气和CO2.
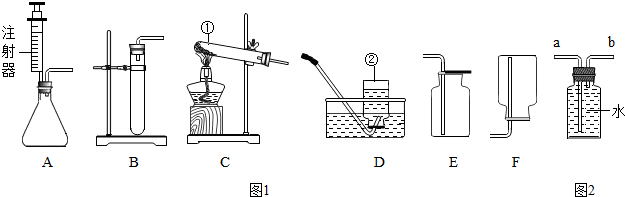
他设法收集了除去醋酸气体的气体样品,用如图1装置验证水蒸气和CO2存在.装置导气管口正确的连接顺序是为:
气体样品→d→c→b→a.
(2)小明对二氧化碳的来源作了两种猜测:
猜测①:二氧化碳可能是由碳酸氢钠与食醋中的醋酸反应产生的.
猜测②:二氧化碳可能是由碳酸氢钠受热分解产生的.
针对以上猜测,小明设计了以下实验:
【实验结论】:猜想①、②都正确
【实验探究二】测定安多夫样品中碳酸氢钠的含量
上述实验2中,小明发现充分反应后,试管中仍留有一些白色固体粉末,通过查阅资料
发现是碳酸钠和氯化钠.小明想用测定白色固体中碳酸钠的质量来推算安多夫样品中碳酸氢钠的含量,于是称取实验2中得到的白色固体粉末6.9g,设计了如图2实验方案:
(1)“操作1”中玻璃棒的作用是引流.
(2)实验中加入过量氯化钙溶液的目的是使碳酸钠完全反应.
(3)确定沉淀A已洗涤干净的方法是取最后一次洗涤液,滴加硝酸银(或碳酸钠)溶液,无沉淀产生.
(4)该安多夫样品中NaHCO3的质量分数是84%.

【查阅资料】
(1)碳酸氢钠是白色细小晶体,加热到50℃以上开始逐渐分解生成碳酸钠、二氧化碳和水,440℃时完全分解.
(2)白色无水硫酸铜遇到水会变成蓝色.
【实验探究一】对烧煮时产生大量气体的探究
(1)小明对气体的成分进行了猜测:气体中除了醋酸气体之外,还可能含有水蒸气和CO2.
他设法收集了除去醋酸气体的气体样品,用如图1装置验证水蒸气和CO2存在.装置导气管口正确的连接顺序是为:
气体样品→d→c→b→a.
(2)小明对二氧化碳的来源作了两种猜测:
猜测①:二氧化碳可能是由碳酸氢钠与食醋中的醋酸反应产生的.
猜测②:二氧化碳可能是由碳酸氢钠受热分解产生的.
针对以上猜测,小明设计了以下实验:
| 实验步骤 | 实验现象 | |
| 实验1 | 取样与试管中,加入食醋,并将产生气体通入澄清石灰水中 | 有气泡产生,石灰水变浑浊 |
| 实验2 | 取安多夫样品少许加入试管中,加热使之充分反应,并把产生的气体通入澄清石灰水 | 试管口出现小水珠,澄清石灰水变浑浊,试管中残留白色固体粉末 |
【实验探究二】测定安多夫样品中碳酸氢钠的含量
上述实验2中,小明发现充分反应后,试管中仍留有一些白色固体粉末,通过查阅资料
发现是碳酸钠和氯化钠.小明想用测定白色固体中碳酸钠的质量来推算安多夫样品中碳酸氢钠的含量,于是称取实验2中得到的白色固体粉末6.9g,设计了如图2实验方案:
(1)“操作1”中玻璃棒的作用是引流.
(2)实验中加入过量氯化钙溶液的目的是使碳酸钠完全反应.
(3)确定沉淀A已洗涤干净的方法是取最后一次洗涤液,滴加硝酸银(或碳酸钠)溶液,无沉淀产生.
(4)该安多夫样品中NaHCO3的质量分数是84%.
6.下列各符号中数字“2”表示的意义不正确的是( )
| A. | 2NO3-:两个硝酸根离子 | |
| B. | N2:一个氮分子由两个氮原子构成 | |
| C. | 2Hg:两个汞原子 | |
| D. | Fe2+:一个铁离子带两个单位的正电荷 |
16.下列厨房中的物品不易溶于水的是( )
| A. | 酱油 | B. | 食盐 | C. | 花生油 | D. | 蔗糖 |
1.下列实验操作正确的是( )
| A. | 闻气体气味 | B. | 稀释浓硫酸 | C. | 倾倒液体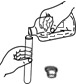 | D. | 读取液体体积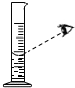 |