题目内容
8.甲、乙、丙三位同学在活动课上利用如图1所示装置制取常见的气体,请根据题意回答下列问题.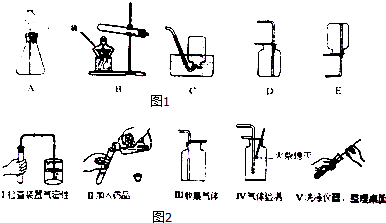
(1)写初编号仪器的名称:a酒精灯
(2)甲同学用高锰酸钾制取O2,发生装置用B装置制取,试管口要放一团棉花,目的是,该反应的化学方程式为,若用C装置收集,当O2收集满并取出集气瓶后,实验结束时的正确操作方法是把导管从水槽中取出后,再移走酒精灯并熄灭.若用该装置收集的氧气不纯,则可能的原因是装置漏气(答一种即可).
(3)乙同学利用A装置抽取CO2,用澄清石灰水检验二氧化碳气体,其反应的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O,如图2是乙同学在化学实验中主要操作过的示意图.
根据上述实验操作过程,请找出乙同学的操作错误的是Ⅱ,Ⅳ(填序号).
(4)实验室常用氯化氨固体与石灰固体共热来制取氨气NH3.常温下NH3是一种无色,有刺激性气味的气体,密度比空气小,极易溶于水,制取并收集NH3,应该从如图1中选择的发生装置和收集装置是BE.(填字线编号)
分析 (1)据常用仪器的名称解答;
(2)高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气;停止该实验时要注意正确的操作顺序;
(3)二氧化碳的实验室制法是用稀盐酸与大理石(或石灰石.其主要成分都是碳酸钙)反应来制取.二氧化碳的检验方法;实验操作得当,能够保证实验顺利完成,操作不当,会影响实验结果,甚至会导致实验失败;
(4)发生装置依据反应物状态及反应条件,收集装置的性质依据气体的密度及溶解性解答;
解答 解:(1)编号仪器的名称是酒精灯;
(2)甲同学用高锰酸钾制取O2,发生装置用B装置制取,试管口要放一团棉花,目的是防止高锰酸钾进入导管,堵塞导管;反应的方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;若用C装置收集,当O2收集满并取出集气瓶后,实验结束时的正确操作方法是把导管从水槽中取出后,再移走酒精灯并熄灭;若用该装置收集的氧气不纯,则可能的原因是装置漏气、收集前试管内没有装满水;
(3)二氧化碳的实验室制法是用稀盐酸与大理石(或石灰石.其主要成分都是碳酸钙)反应来制取,反应不需加热,发生装置选择A;用澄清石灰水检验二氧化碳气体,其反应的化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O;加入药品时,瓶塞正放在桌上,这样容易沾上杂质,会污染试剂,是错误的;
二氧化碳验满时,因为二氧化碳的密度比空气大,燃烧的火柴伸入集气瓶中,如果没有收集满,也可能导致火柴熄灭,是错误的;
检查装置气密性、收集气体、洗涤仪器等都是正确的
(4)实验室常用氯化氨固体与石灰固体共热来制取氨气NH3,反应需加热,发生装置选择B;常温下NH3是一种无色,有刺激性气味的气体,密度比空气小,极易溶于水,只能用向下排空气法收集.
故答案为:(1)酒精灯;(2)防止高锰酸钾进入导管,堵塞导管、2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑、把导管从水槽中取出后,再移走酒精灯并熄灭、装置漏气;
(3)A、CO2+Ca(OH)2=CaCO3↓+H2O、Ⅱ,Ⅳ;(4)BE.
点评 二氧化碳不能使石蕊试液变色,二氧化碳的水溶液能使石蕊试液变红色,是因为二氧化碳和水反应生成了碳酸的缘故.

| 物质 | 所含杂质 | 所加药品 | 用量 | 操作 | |
| A | NaCl溶液 | NaOH和Na2CO3 | 稀盐酸 | 适量 | 加稀盐酸至恰好不再产生气泡 |
| B | CuO粉末 | C | 稀盐酸 | 足量 | 加入稀盐酸充分反应后过滤 |
| C | Cu | CuCl2固体 | 水 | 适量 | 加水搅拌后,过滤 |
| D | K2SO4 | CuSO4 | 氢氧化钾溶液 | 适量 | 加入适量氢氧化钾溶液,蒸发 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 石油分馏可得到汽油、煤油等多种产品,属于化学变化 | |
| B. | 只有产生燃烧的化学反应才会放热 | |
| C. | 氧化反应都会放出热量 | |
| D. | 能量都是由化学反应产生的 |
| 选项 | 物质(括号内为杂质) | 除去杂质的方法 |
| A | NaOH溶液(Na2CO3) | 加入适量的Ca(OH)2溶液、过滤 |
| B | CaO(CaCO3) | 加水溶解、过滤 |
| C | CO(CO2) | 通过足量的NaOH溶液、干燥 |
| D | FeSO4溶液(H2SO4) | 加入足量Fe粉、过滤 |
| A. | A | B. | B | C. | C | D. | D |

 如图是某化学反应的微观示意图,从图中获得的有关信息正确的是A.
如图是某化学反应的微观示意图,从图中获得的有关信息正确的是A. 和
和 的分子个数比为2:1
的分子个数比为2:1