题目内容
18.我国化学家侯德榜发明了联合制碱法,其生产纯碱和副产品氯化铵的工艺流程如图所示: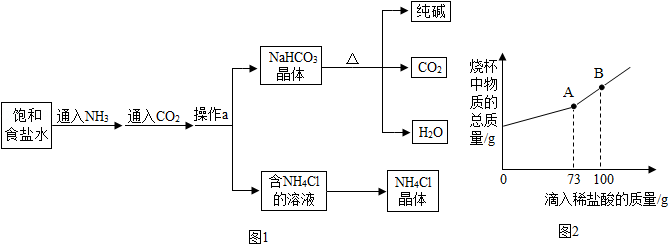
请回答下列问题:
(1)操作a的名称是过滤;
(2)上述工艺流程中可循环利用的物质是二氧化碳(填名称).
(3)铵盐水吸收二氧化碳后生成碳酸氢钠和氯化铵,碳酸氢钠首先结晶析出,原因是相同条件下碳酸氢钠的溶解度较小.
(4)某制碱厂制出的Na2CO3中含有NaCl,取12g该样品放入烧杯中,逐渐滴加溶质质量分数为10%的稀盐酸,烧杯中物质的总质量与所滴入稀盐酸的质量关系曲线如图所示,当恰好完全反应时,烧杯中为不饱和溶液,试通过计算求出此时溶液中所含溶质的质量.
分析 碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳,根据反应的化学方程式及其提供的数据可以进行相关方面的计算和判断.
解答 解:(1)操作a的名称是过滤,通过过滤把液体和固体分离.
故填:过滤.
(2)上述工艺流程中可循环利用的物质是二氧化碳.
故填:二氧化碳.
(3)铵盐水吸收二氧化碳后生成碳酸氢钠和氯化铵,碳酸氢钠首先结晶析出,原因是相同条件下碳酸氢钠的溶解度较小.
故填:相同条件下碳酸氢钠的溶解度较小.
(4)解:设Na2CO3的质量为x,反应后生成NaCl的质量为y,
Na2CO3+2HCl=H2O+CO2↑+2NaCl,
106 73 117
x 73g×10% y
$\frac{106}{x}$=$\frac{73}{73g×10%}$=$\frac{117}{y}$,
x10.6g,y=11.7g,
此时溶液中所含溶质的质量为:12g-10.6g+11.7g=13.1g,
答:溶液中所含溶质的质量为13.1g.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
8.化学与人体健康密切相关.市场上有“高钙牛奶”、“加氟牙膏”、“葡萄糖酸锌”等商品,这里的钙、氟、
锌应理解为( )
锌应理解为( )
| A. | 元素 | B. | 原子 | C. | 分子 | D. | 离子 |
6.食品安全关系到人民的健康,下列属于安全食品的是( )
| A. | 用甲醛浸泡的韭菜 | B. | 用生霉的大米制作米粉 | ||
| C. | 加入化工染料苏丹红的辣椒酱 | D. | 加入适量碳酸氢钠焙制的面包 |
10.下列表中的叙述,对应的化学方程式和所属反应基本类型都正确的是( )
| 选项 | 叙述 | 化学反应方程式 | 反应类型 |
| A | 电解水 | 2H2O$\frac{\underline{\;通电\;}}{\;}$H2↑+O2↑ | 分解反应 |
| B | 探究一氧化碳的还原性 | 3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | 置换反应 |
| C | 酸雨形成的原因 | CO2+H2O═H2CO3 | 化合反应 |
| D | 硫酸铜溶液中滴加氢氧化钠溶液 | CuSO4+2NaOH═Na2SO4+Cu(OH)2↓ | 复分解反应 |
| A. | A | B. | B | C. | C | D. | D |
7.为测定某黄铜(铜、锌合金)中铜的质量分数,称取32.5g该黄铜粉末放入烧杯中,再向烧杯内加入200g稀硫酸(足量),每隔10分钟测烧杯内(不含烧杯)剩余物质的质量,测得数据如表:
(1)完全反应后生成氢气的质量为0.4g.
(2)计算该黄铜中铜的质量分数(写出计算过程).
| 加入稀硫酸后10分钟 | 加入稀硫酸后20分钟 | 加入稀硫酸后 | 加入稀硫酸后40分钟 | 加入稀硫酸后50分钟 |
| 232.4g | 232.3g | 232.2g | 232.1g | 232.1g |
(2)计算该黄铜中铜的质量分数(写出计算过程).
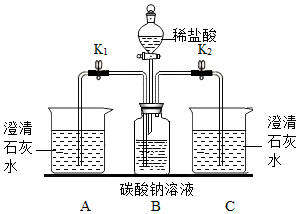
8.某化学兴趣小组用下图装置进行Na2CO3的性质实验.
【实验装置】
【实验记录】
【反思与交流】
1、实验后,同学们分析实验Ⅲ中B瓶溶液的溶质为NaCl和Na2CO3.
2、某同学向B瓶中继续加入稀盐酸,发现A中白色沉淀消失且红色褪去,白色沉淀消失的原因为CaCO3+2HCl=CaCl2+H2O+CO2↑(用化学方程式表示).
【实验装置】

【实验记录】
| 实验步骤 | 实验现象 | 实验结论 | |
| Ⅰ | 向B瓶中滴入几滴酚酞试液 | B瓶中溶液变红 | Na2CO3溶液呈碱性 |
| Ⅱ | 关闭开关K1,打开K2,并加入一定量稀盐酸 | B中有气泡;C中 澄清石灰水变浑浊 | Na2CO3与稀盐酸反应 |
| Ⅲ | 关闭开关K2,打开K1 | ①B瓶中液体压入A中 ②A中产生白色沉淀,且溶液变红 | A中发生反应的化学方程式: Na2CO3+Ca(OH)2=CaCO3↓+2NaOH |
1、实验后,同学们分析实验Ⅲ中B瓶溶液的溶质为NaCl和Na2CO3.
2、某同学向B瓶中继续加入稀盐酸,发现A中白色沉淀消失且红色褪去,白色沉淀消失的原因为CaCO3+2HCl=CaCl2+H2O+CO2↑(用化学方程式表示).
 (1)根据《食用盐国家标准》,食盐是无异味的,然而,近日多地却出现了让人恶心的“脚臭盐”,该批次盐不仅味道难闻,经检测该盐中还含有毒,有害成分亚硝酸盐,由此断定“脚臭盐”属于混合物(填“有机物”、“混合物”、“纯净物”之一);
(1)根据《食用盐国家标准》,食盐是无异味的,然而,近日多地却出现了让人恶心的“脚臭盐”,该批次盐不仅味道难闻,经检测该盐中还含有毒,有害成分亚硝酸盐,由此断定“脚臭盐”属于混合物(填“有机物”、“混合物”、“纯净物”之一);