题目内容
4. A、B、C、D、E分别为初中化学常见的物质,它们之间的反应或转化关系如图所示(部分物质和反应条件已略去),其中A是一种碱,E为Fe,C是人体胃液中的主要成分,B是石灰石的主要成分,请回答下列问题.
A、B、C、D、E分别为初中化学常见的物质,它们之间的反应或转化关系如图所示(部分物质和反应条件已略去),其中A是一种碱,E为Fe,C是人体胃液中的主要成分,B是石灰石的主要成分,请回答下列问题.(1)C的化学式为HCl.
(2)请写出一个符合反应①的化学方程式Ca(OH)2+Na2CO3=CaCO3↓+2NaOH.
(3)A在生产或生活中的一种用途是改良酸性土壤.
分析 根据A、B、C、D、E分别为初中化学常见的物质,A是一种碱,E为Fe,C是人体胃液中的主要成分,所以C是盐酸,B是石灰石的主要成分,所以B是碳酸钙,A会转化成碳酸钙,所以A是氢氧化钙,D会转化成铁,会与盐酸反应,所以D是氧化铁,然后将推出的物质进行验证即可.
解答 解:(1)A、B、C、D、E分别为初中化学常见的物质,A是一种碱,E为Fe,C是人体胃液中的主要成分,所以C是盐酸,B是石灰石的主要成分,所以B是碳酸钙,A会转化成碳酸钙,所以A是氢氧化钙,D会转化成铁,会与盐酸反应,所以D是氧化铁,经过验证,推导正确,所以C是HCl;
(2)反应①是氢氧化钙和碳酸钠反应生成碳酸钙沉淀嗯哼氢氧化钠,化学方程式为:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
(3)A在生产或生活中的一种用途是改良酸性土壤.
故答案为:(1)HCl;
(2)Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
(3)改良酸性土壤.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.下列关于水的说法中,错误的是( )
| A. | 生活中饮用的矿泉水属于混合物 | B. | 二氧化碳与水混合时水仅作溶剂 | ||
| C. | 水通电分解时能产生氢气和氧气 | D. | 水是人体必不可少的一种营养素 |
12.下列对生活中常见现象的解释,正确的是( )
| A. | 冬天用热水杯捂手,手一会就变暖和了,说明手的热量传递给了水 | |
| B. | 将一勺白糖放入一杯水中,整杯水都变甜了,说明分子是不断地运动的 | |
| C. | 寒冷的冬天,水会结成冰,此时分子的种类发生了变化 | |
| D. | 用手压海绵,海绵很容易被压扁了,说明分子之间不存在斥力 |
19.下列实验操作正确的是( )
| A. | 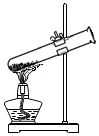 加热胆矾固体 | B. | 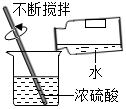 稀释浓硫酸 | ||
| C. | 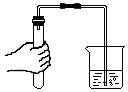 检查装置的气密性 | D. | 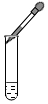 滴加液体试剂 |
9.化学知识可以解决许多实际问题,如表中完全正确的一组是( )
| A. | 安全常识 | B. | 数据记录 |
| 天然气泄漏立即打开换气扇 炒菜时油锅着火-用锅盖盖灭 预防煤气中毒-确保烟道畅通 | 量筒量液体-体积为9.1ml 托盘天平称固体-质量为5.2g pH试纸测酸雨-pH为4.5 | ||
| C. | 物质的性质与用途 | D. | 化学反应的条件 |
| N2化学性质稳定-作保护气 H2具有可燃性-作气体燃料 CO具有还原性-冶炼金属 | 实验室制氧气-一定需要催化剂 燃烧-接触氧气,温度达到着火点 复分解反应-生成气体、沉淀或水 |
| A. | A | B. | B | C. | C | D. | D |
16.同学们对制作糕点常用膨松剂Na2CO3或NaHCO3进行了下列探究.
【查阅资料】
【探究一】
Ⅰ.NaHCO3和Na2CO3性质差异的探究
(1)现有20℃时溶质质量分数为8%的Na2CO3和NaHCO3溶液
酸碱性:取样于试管中,分别滴加紫色石蕊试液,均显红色;
酸碱度:NaHCO3溶液<Na2CO3溶液(填“>”或”“<”).
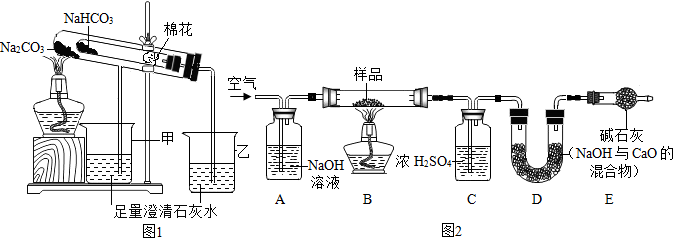
(2)稳定性:按图1,实验中可观察乙烧杯中的石灰水变浑浊,对应试管中发生反应的化学方程式为:CO2+Ca(OH)2═CaCO3↓+H2O.
结论:在受热条件下,碳酸钠比碳酸氢钠稳定性强(填“强”或“弱”).
(3)利用溶解度鉴别NaHCO3和Na2CO3:分别取Xg两种固体粉末加入20℃,10g水中充分溶解,通过观察溶解现象来区分,X可以是下列的A.(选填A、B或C)
A.2g B.0.96g C.0.5g
Ⅱ.测定NaHCO3和Na2CO3混合物10.0g中NaHCO3的质量分数(图2,夹持装置略)
【问题讨论】
(4)实验前先通一段时间的空气的目的是排尽装置内的空气(或二氧化碳);
(5)A的作用是吸收鼓入空气中的二氧化碳,若没有装置E,NaHCO3的质量分数测定结果会偏大(填“偏大”、“不变”或“偏小”).
(6)停止加热后,仍继续通入空气一段时间,目的是使反应生成的二氧化碳全部被D吸收.
【含量测定】
(7)测得装置D的质量实验前为120.2g,实验后为122.4g,计算该样品中NaHCO3的质量分数.(要有计算过程)
【知识拓展】
(8)向Na2CO3溶液中通入CO2气体可以生成NaHCO3,该反应的化学反应方程式为:Na2CO3+CO2+H2O═2NaHCO3.
【查阅资料】
| 20℃ | 8%Na2CO3溶液 | 8%NaHCO3溶液 |
| pH | 10.6 | 8.0 |
| 溶解度 | 10℃ | 20℃ | 30℃ | 40℃ |
| Na2CO3 | 12.5g | 21.5g | 39.7g | 49.0g |
| NaHCO3 | 8.1g | 9.6g | 11.1g | 12.7g |
Ⅰ.NaHCO3和Na2CO3性质差异的探究
(1)现有20℃时溶质质量分数为8%的Na2CO3和NaHCO3溶液
酸碱性:取样于试管中,分别滴加紫色石蕊试液,均显红色;
酸碱度:NaHCO3溶液<Na2CO3溶液(填“>”或”“<”).
(2)稳定性:按图1,实验中可观察乙烧杯中的石灰水变浑浊,对应试管中发生反应的化学方程式为:CO2+Ca(OH)2═CaCO3↓+H2O.
结论:在受热条件下,碳酸钠比碳酸氢钠稳定性强(填“强”或“弱”).
(3)利用溶解度鉴别NaHCO3和Na2CO3:分别取Xg两种固体粉末加入20℃,10g水中充分溶解,通过观察溶解现象来区分,X可以是下列的A.(选填A、B或C)
A.2g B.0.96g C.0.5g
Ⅱ.测定NaHCO3和Na2CO3混合物10.0g中NaHCO3的质量分数(图2,夹持装置略)
【问题讨论】
(4)实验前先通一段时间的空气的目的是排尽装置内的空气(或二氧化碳);
(5)A的作用是吸收鼓入空气中的二氧化碳,若没有装置E,NaHCO3的质量分数测定结果会偏大(填“偏大”、“不变”或“偏小”).
(6)停止加热后,仍继续通入空气一段时间,目的是使反应生成的二氧化碳全部被D吸收.
【含量测定】
(7)测得装置D的质量实验前为120.2g,实验后为122.4g,计算该样品中NaHCO3的质量分数.(要有计算过程)
【知识拓展】
(8)向Na2CO3溶液中通入CO2气体可以生成NaHCO3,该反应的化学反应方程式为:Na2CO3+CO2+H2O═2NaHCO3.

14.下列微粒结构示意图中,说法错误的是( )
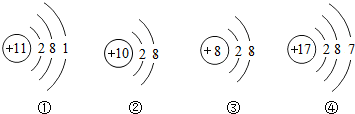
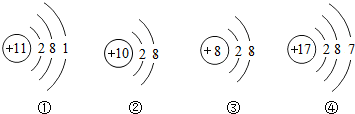
| A. | ①在化合物中的化合价通常为+1 价 | B. | ②的化学性质比较稳定 | ||
| C. | ③是一种阳离子 | D. | ④容易得到电子 |