题目内容
7.镁是叶绿素中唯一的金属元素.植物缺镁时,通常的症状表现为叶片失绿,严重 时整片叶干枯.给农作物加MgSO4和NH4MgPO4(磷酸镁铵)等镁肥,可以促进光合作用,提高抗病能力.(1)NH4MgPO4中N、H、O的原子个数比是1:4:4,NH4MgPO4由5种元素组成
(2)现要配制溶质量分数为2%的MgSO4溶液500kg进行喷施,需25%的MgSO4溶液的质量是40kg.
分析 (1)根据化学式的意义来分析;
(2)根据加水稀释前后溶液中学界质质量不变,溶质质量分数为2%的MgSO4溶液500kg中所含MgSO4的质量与质量分数25%的比,即需25% MgSO4溶液的质量.
解答 解:(1)由化学式NH4MgPO4可知,NH4MgPO4中N、H、O的原子个数比是1:4:4,NH4MgPO4由五种种元素组成;故填:1:4:4;5;
(2)设需25%MgSO4溶液的质量是x
500kg×2%=x×25% 解得:x=40kg.
故填:40.
点评 本题属于化学中的基础计算,难度不大,注意计算数据的准确性.

练习册系列答案
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案
相关题目
17.在研究酸和碱的化学性质时,某小组想证明稀硫酸与氢氧化钠溶液混合后,虽然无明显现象,但确实发生了化学反应,试与他们一起完成实验方案的设计,实施和评价,并得出有关结论.
(1)探究稀硫酸与氢氧化钠溶液的反应:
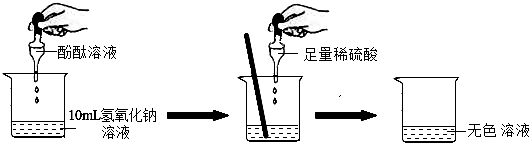
根据上述实验中颜色变化,可确定稀硫酸与氢氧化钠溶液发生了化学变化,反应的化学方程式为:2NaOH+H2SO4=Na2SO4+2H2O.
(2)探究上述稀硫酸与氢氧化钠溶液反应后烧杯中的硫酸是否过量:
根据上述反应过程中溶液变成无色,不能确定稀硫酸是否过量,同学们又分别选取氯化钡溶液、紫色石蕊试液设计实验方案,请你判断并分析:
上述设计的实验方案中,正确的是方案二(填“方案一”或“方案二”)
另外一个实验方案错误的原因是NaOH和H2SO4反应后生成的硫酸钠也能和BaCl2反应产生白色沉淀BaSO4;
请你设计一个确定稀硫酸是否过量的实验方案,你选用的药品是锌粒(或碳酸钠等),实验现象及结论是若有气体放出,证明稀硫酸过量,反之稀硫酸不过量.
(1)探究稀硫酸与氢氧化钠溶液的反应:

根据上述实验中颜色变化,可确定稀硫酸与氢氧化钠溶液发生了化学变化,反应的化学方程式为:2NaOH+H2SO4=Na2SO4+2H2O.
(2)探究上述稀硫酸与氢氧化钠溶液反应后烧杯中的硫酸是否过量:
根据上述反应过程中溶液变成无色,不能确定稀硫酸是否过量,同学们又分别选取氯化钡溶液、紫色石蕊试液设计实验方案,请你判断并分析:
| 实验方案 | 实验步骤 | 实验现象 | 实验结论 |
| 方案一 | 取样,滴入适量的氯化钡溶液 | 出现白色沉淀 | 稀硫酸过量 |
| 方案二 | 取样,滴入几滴紫色石蕊试液 | 溶液变红 | 稀硫酸过量 |
另外一个实验方案错误的原因是NaOH和H2SO4反应后生成的硫酸钠也能和BaCl2反应产生白色沉淀BaSO4;
请你设计一个确定稀硫酸是否过量的实验方案,你选用的药品是锌粒(或碳酸钠等),实验现象及结论是若有气体放出,证明稀硫酸过量,反之稀硫酸不过量.
18.物质的性质决定了物质的用途.下列物质的用途由其物理性质决定的是( )
| A. | 焦炭冶炼金属 | B. | 氩气用作电焊时的保护气 | ||
| C. | 潜水员潜水时携带氧气瓶 | D. | 干冰用于人工降雨 |
15.一位学生要用托盘天平称量12.5g药品,在称量中发现指针向左偏转,这时他应该( )
| A. | 增加药品 | B. | 减少药品 | C. | 移动游码 | D. | 向右盘中加法码 |
19.下列对原子、分子、离子的认识,错误的是( )
| A. | 分子由原子构成,原子是不能再分的最小粒子 | |
| B. | 相同原子可以构成不同的分子 | |
| C. | 在原子中,原子核内的质子数等于核外电子数 | |
| D. | 分子、原子、离子都是构成物质的粒子 |
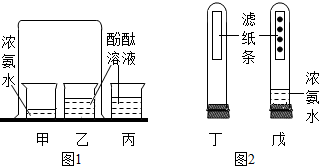 小红同学对探究分子性质的实验(图1)进行了改进.如图2所示,试管丁、戊中各有一张每隔2厘米滴有一滴酚酞溶液的滤纸条,试管戊中装有适量浓氨水的小药瓶固定在橡皮塞上,小药瓶上无瓶塞.关于实验有以下说法,其中说法正确的是( )
小红同学对探究分子性质的实验(图1)进行了改进.如图2所示,试管丁、戊中各有一张每隔2厘米滴有一滴酚酞溶液的滤纸条,试管戊中装有适量浓氨水的小药瓶固定在橡皮塞上,小药瓶上无瓶塞.关于实验有以下说法,其中说法正确的是( )